合作客户/
拜耳公司 |
同济大学 |
联合大学 |
美国保洁 |
美国强生 |
瑞士罗氏 |
相关新闻Info
-
> 基于界面张力和流变测试研究SiO_2纳米颗粒对各表面活性剂体系性能的影响
> 烷基二苯醚/烷基苯混合磺酸盐静态表面张力、金属腐蚀性及净洗力测定(一)
> 液滴撞击固体表面过程中黏度与表面张力系数变化(一)
> 海藻糖脂:一种兼具优异发泡性能与皮肤温和性的新型表面活性剂(二)
> 影响狭缝间氢键流体气液平衡界面张力的因素有哪些(一)
> 各种共存阳离子的水化能力、稀土萃取过程的界面盐效应微观机制研究
> 手机实验软件测量液体表面张力系数VS传统实验效果比较
> 含氟防水防油剂的基础理论知识分享
> 新型多功能解堵体系-单相酸体系乳化、界面张力测定及现场应用效果(一)
> 拉筒法和静滴法测定连铸结晶器保护渣表面张力(一)
推荐新闻Info
-
> 动态表面张力与界面特性关联研究:揭示AE2S在高矿化度环境中的泡沫优越性
> 超微量天平在三类主流化学分析中的称量应用与实测数据、控制方案
> 兼具高耐盐性与高表面活性:一种双阴非表面活性剂的制备与表征
> 双醚键合型阴非离子表面活性剂的合成优化、结构表征与构效关系
> 界面扩张黏弹性与驱油机理研究进展
> 蛋白质聚集与表面张力:界面行为、聚集机制及测量技术前沿
> 动态光散射法(DLS)在临界胶束浓度(CMC)测定中的原理、应用与最新进展
> 溶液吸附作用与表面张力测定:从理论到实践的完整指南
> 面向水基农药制剂的新型表面活性剂TPGS-X-M动静态表面张力及性能研究
> 表面活性剂TPGS-X-M的合成及表面张力测试
血脑屏障概述
来源:丁香叶 浏览 3380 次 发布时间:2022-09-21
血脑屏障(BBB)是一种高度选择性的半透性边界,可将循环血液与脑和中枢神经系统(CNS)中的细胞外液分开。[1]血脑屏障由毛细血管壁的内皮细胞,包裹毛细血管的星形胶质细胞末端和嵌入毛细血管基底膜的周细胞形成。[2]该系统允许一些分子通过被动扩散通过,以及选择性运输对神经功能至关重要的分子,如葡萄糖,水和氨基酸。
参与神经回路内感觉和分泌整合的专门结构-周围器官和脉络丛-没有血脑屏障。[3]
血脑屏障限制了病原体的通过,溶质在血液中的扩散,以及大或亲水分子进入脑脊液(CSF),同时允许疏水分子(O2,CO2,激素)和小极性分子的扩散[4]。屏障细胞使用特定的转运蛋白主动将代谢产物如葡萄糖转运穿过屏障。[5]
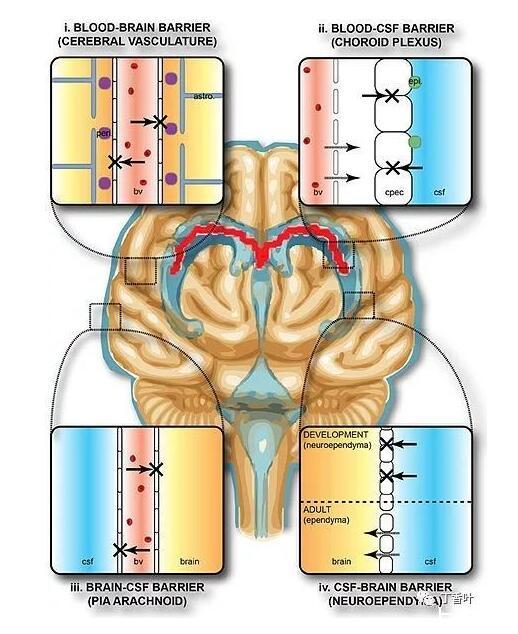
血液和脑脊液脑屏障
关系
从技术上讲,BBB是血液-中枢神经系统屏障的简写,它有两个部分:血脑部分和血脊髓屏障部分。这两个部分经常被同时破坏,但可能会被独立破坏。
结构体
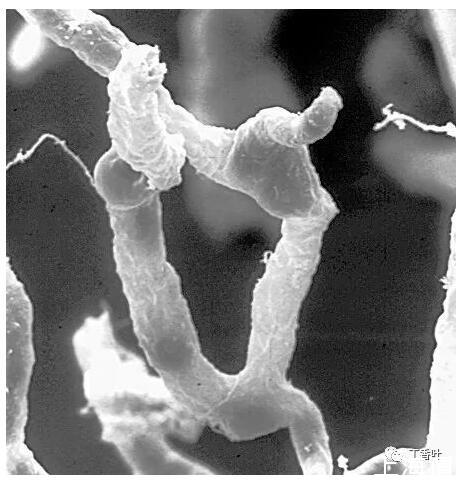
供应脑细胞的毛细血管网络的一部分
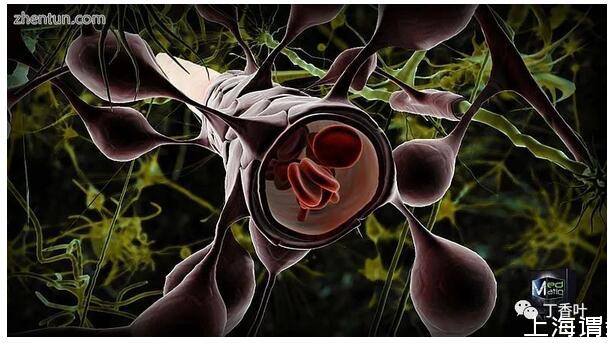
星形胶质细胞1型包围大脑中的毛细血管
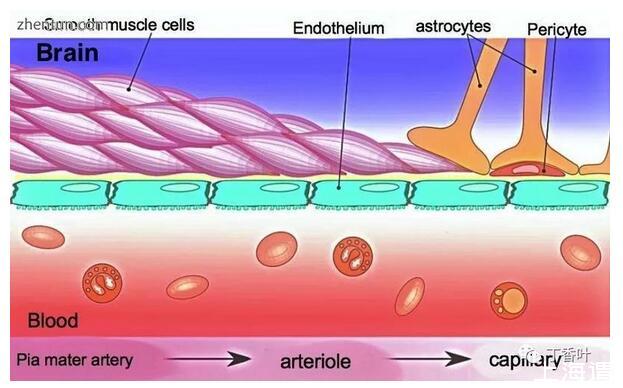
草图显示大脑内血管的构成
血脑屏障是由CNS血管中内皮细胞之间紧密连接的选择性引起的,这限制了溶质的通过[1]。在血液和大脑之间的界面处,内皮细胞通过这些紧密连接缝合在一起,这些连接由较小的亚基组成,通常是生物化学二聚体,它们是跨膜蛋白,如occludin,claudins,连接粘附分子(JAM)或ESAM,例如。[5]这些跨膜蛋白中的每一种都被另一种包含ZO-1和相关蛋白的蛋白质复合物锚定在内皮细胞中。[5]
血脑屏障由高密度细胞组成,这些细胞限制物质从血液中通过,远远超过身体其他部位毛细血管中的内皮细胞。[6]称为星形细胞足(也称为“胶质细胞限制因子”)的星形胶质细胞突起围绕BBB的内皮细胞,为这些细胞提供生化支持。[7]BBB不同于非常相似的血-脑脊液屏障,它是脉络丛的脉络膜细胞和血-视网膜屏障的功能,可以被认为是这些屏障的整个领域的一部分。8]
人脑的几个区域不在BBB的大脑侧。这方面的一些例子包括周围器官,第三和第四脑室的顶部,在间脑顶上的松果腺中的毛细血管和松果体。松果体分泌激素褪黑激素“直接进入体循环”,[9]因此褪黑激素不受血脑屏障的影响。[10]
发展
最初,20世纪20年代的实验似乎(错误地)表明血脑屏障(BBB)在新生儿中仍然不成熟。这是由于方法学上的错误(渗透压太高而脆弱的胚胎毛细血管部分受损)。后来在实验中显示注射液体积减少,所研究的标记物无法通过BBB。据报道,在脑内细胞外无法检测到新生儿血浆浓度升高的白蛋白,α-1-甲胎蛋白或转铁蛋白等天然物质。转运蛋白P-糖蛋白已经存在于胚胎内皮中。[11]
在乙醚麻醉的新生兔与成年兔中测量乙酰胺,安替比林,苯甲醇,丁醇,咖啡因,胞嘧啶,苯妥英,乙醇,乙二醇,海洛因,甘露醇,甲醇,苯巴比妥,丙二醇,硫脲和尿素的脑摄取表明新生兔和成年兔脑内皮细胞在脂质介导的通透性方面功能相似[12]。这些数据证实,在新生儿和成人BBB毛细血管之间没有检测到渗透性差异。在成年兔和新生兔之间没有观察到大脑摄取葡萄糖,氨基酸,有机酸,嘌呤,核苷或胆碱的差异。[12]这些实验表明,新生儿BBB具有与成人相似的限制性质。与年幼动物不成熟屏障的建议相反,这些研究表明,复杂的,有选择性的BBB在出生时是有效的。
功能
另见:神经免疫系统
血脑屏障有效地保护大脑免受循环病原体的侵害。因此,大脑的血源性感染是罕见的。[1]确实发生的大脑感染通常很难治疗。抗体太大而无法穿过血脑屏障,只有某些抗生素才能通过。[13]在某些情况下,药物必须直接注入脑脊液(CSF),在那里它可以通过穿过血-脑脊液屏障进入大脑。[14][15]
选择性神经系统疾病,如肌萎缩侧索硬化,癫痫,脑外伤和水肿,以及全身性疾病,如肝功能衰竭,血脑屏障可能会渗漏。[1]血脑屏障在炎症期间变得更具渗透性,[1]允许抗生素和吞噬细胞穿过BBB。然而,这也使细菌和病毒渗入血脑屏障。[13][16]可以穿过血脑屏障的病原体的实例包括导致弓形虫病的弓形虫,像疏螺旋体(莱姆病)的螺旋体,在新生儿中引起脑膜炎的B组链球菌,[17]和引起梅毒的梅毒螺旋体。这些有害细菌中的一些通过释放细胞毒素如肺炎球菌溶血素[18]获得进入,这些细胞毒素对脑微血管内皮[19]和紧密连接具有直接毒性作用。
脑室周围器官
主要文章:室旁器官
室旁器官(CVO)是位于大脑第四脑室或第三脑室附近的个体结构,其特征是毛细血管密集的床具有可渗透的内皮细胞,不像血脑屏障。[20][21]具有高渗透性毛细血管的CVO包括后区,穹窿下器官,椎板末端血管器官,中位隆起,松果腺和脑垂体的三个叶。[20][22]
感觉CVO的渗透性毛细血管(后区域,穹窿下器官,椎板的血管器官)能够快速检测全身血液中的循环信号,而分泌型CVO(中位隆起,松果腺,垂体叶)的毛细血管促进脑的运输。-来自循环血液的信号。[20][21]因此,CVO可渗透毛细血管是神经内分泌功能的双向血脑通信点。[20][22][23]
专业的渗透区
在血脑屏障“后面”的脑组织和某些CVO中“开放”血液信号的区域之间的边界区域包含比典型的脑毛细血管更漏的专用混合毛细血管,但不像CVO毛细血管那样具有渗透性。这些区域存在于postrema-nucleus tractus solitarii(NTS),[24]和中位隆起-下丘脑弓状核区域的边界。[23][25]这些区域似乎充当了涉及多种神经回路的大脑结构的快速转运区域-如NTS和弓状核-以快速控制神经体液整合[需要澄清]。[23][24]中位隆起和下丘脑弓状核之间共享的可渗透毛细血管区域由宽的毛细血管间隙增强,促进两个结构之间的溶质双向流动,并且表明中位隆起不仅是分泌器官,还可能是感觉CVO。[23]。[25]
临床意义
作为药物目标
血脑屏障(BBB)由脑毛细血管内皮形成,并从大脑中排除~100%的大分子神经治疗药物和98%以上的小分子药物。[1]克服将治疗剂递送到大脑的特定区域的困难对大多数脑疾病的治疗提出了主要挑战。在其神经保护作用中,血脑屏障起到阻碍许多潜在重要的诊断和治疗剂向大脑的递送的作用。否则可能在诊断和治疗中有效的治疗性分子和抗体不会以足够的量穿过BBB。
大脑中药物靶向的机制涉及到BBB“通过”或“后面”。通过BBB以单位剂量向大脑递送药物的方式需要通过渗透方法破坏,或通过使用血管活性物质如缓激肽[26]或甚至通过局部暴露于高强度聚焦超声(HIFU)进行生物化学破坏。[27]用于通过BBB的其他方法可能需要使用内源性转运系统,包括载体介导的转运蛋白如葡萄糖和氨基酸载体,受体介导的胰岛素或转铁蛋白转胞吞作用,以及阻断活性外排转运蛋白如p-糖蛋白。然而,已经发现靶向BBB转运蛋白的载体,例如转铁蛋白受体,仍然被包裹在毛细血管的脑内皮细胞中,而不是通过BBB运送到目标区域。[28][29]药物递送的方法BBB包括脑内植入(例如用针)和对流增强分布。甘露醇可用于绕过BBB。
纳米粒子
主要文章:用于向大脑输送药物的纳米颗粒
纳米技术也可能有助于跨BBB转移药物。[30][31]最近,研究人员一直在尝试制造载有纳米颗粒的脂质体,以便通过BBB进入。需要更多的研究来确定哪种策略最有效,以及如何改善脑肿瘤患者的治疗策略。刚开始探索使用BBB开放将特定药剂靶向脑肿瘤的可能性。
跨越血脑屏障传递药物是纳米技术在临床神经科学中最有希望的应用之一。纳米粒子可能以预定义的顺序执行多个任务,这对于跨越血脑屏障的药物递送非常重要。
该领域的大量研究已经花费在探索纳米颗粒介导的抗肿瘤药物递送至中枢神经系统肿瘤的方法上。例如,放射性标记的聚乙二醇涂覆的十六烷基氰基丙烯酸酯纳米球靶向并积聚在大鼠胶质肉瘤中。[32]然而,由于纳米球在周围健康组织中的积累,该方法尚未准备用于临床试验。另一种更有希望的方法是用聚山梨醇酯80或泊洛沙姆188涂覆聚烷基氰基丙烯酸酯或聚乳酸-共-羟基乙酸(PLGA)纳米颗粒。由于这种涂层,颗粒从血液中吸附载脂蛋白E或A-1,从而相互作用使用信号蛋白LRP1或清道夫受体,然后通过血脑屏障进入大脑的转胞吞作用。[33]这些载有阿霉素的颗粒用于治疗胶质母细胞瘤目前处于临床阶段I.最近,已经发现了一类新的多功能纳米粒子,称为磁电纳米粒子(MENs),用于外部控制的靶向递送和药物的释放。BBB以及大脑深处细胞的无线刺激。这种方法更多地取决于现场控制而不是细胞微环境。佛罗里达国际大学(FIU)的Sakhrat Khizroev教授的研究小组已经进行了体外和体内(小鼠)实验,以证明使用MENs在BBB上按需释放药物并无线刺激大脑的可行性。[34]
血管内皮细胞和相关的周细胞通常在肿瘤中是异常的,并且血脑屏障在脑肿瘤中可能并不总是完整的。而且,基底膜有时是不完整的。其他因素,如星形胶质细胞,可能有助于脑肿瘤对治疗的抵抗。[35][36]
肽
肽能够通过各种机制穿过血脑屏障(BBB),开辟了新的诊断和治疗途径。[37]然而,他们的BBB运输数据分散在不同学科的文献中,使用报告不同流入或流出方面的不同方法。因此,构建了综合的BBB肽数据库(Brainpeps)以收集文献中可获得的BBB数据。Brainpeps目前包含BBB传输信息,包括正面和负面结果。该数据库是优先选择肽选择以评估不同BBB反应或研究肽的定量结构-性质(BBB行为)关系的有用工具。因为已经使用多种方法来评估化合物的BBB行为,所以这些方法及其响应被分类。此外,不同的BBB运输方法之间的关系已得到澄清和可视化。[38]
Casomorphin是一种七肽,能够通过BBB。[39]
疾病
脑膜炎
脑膜炎是围绕脑和脊髓的膜的炎症(这些膜被称为脑膜)。脑膜炎最常见的是由各种病原体感染引起,其实例是肺炎链球菌和流感嗜血杆菌。当脑膜发炎时,血脑屏障可能会被破坏。[13]这种破坏可能会增加各种物质(包括毒素或抗生素)进入大脑的渗透。用于治疗脑膜炎的抗生素可能通过从细菌细胞壁释放神经毒素(如脂多糖(LPS))来加重中枢神经系统的炎症反应。[40]根据致病病原体,无论是细菌,真菌还是原生动物,通常都会使用第三代或第四代头孢菌素或两性霉素B治疗。[41]
脑脓肿
与其他脓肿一样,脑或脑脓肿是由炎症和淋巴细胞的收集以及源自局部或远程感染的感染物质引起的。脑脓肿是一种罕见的危及生命的疾病。当地来源可能包括耳部感染,口腔和牙齿,鼻旁窦或硬膜外脓肿。远程来源可能包括肺,心脏或肾脏感染。脑脓肿也可能由头部创伤或手术并发症引起。在儿童中,脑脓肿通常与先天性心脏病有关。[42]在大多数情况下,需要8-12周的抗菌治疗。[13]
癫痫
癫痫是一种常见的神经系统疾病,其特征是反复发作且有时无法治愈的癫痫发作。一些临床和实验数据表明,血脑屏障功能未能引发慢性或急性癫痫发作[43][44][45][46][47]。一些研究暗示了普通血液蛋白(白蛋白)和星形胶质细胞之间的相互作用。[48]这些发现表明,急性癫痫发作是通过人工或炎症机制破坏BBB的可预测结果。此外,BBB中耐药分子和转运蛋白的表达是对常用抗癫痫药物耐药的重要机制。[49][50]
多发性硬化症
多发性硬化症(MS)被认为是一种自身免疫和神经退行性疾病,其中免疫系统攻击髓鞘,保护和电绝缘中枢和外周神经系统的神经元。通常,由于血脑屏障,白细胞不能接近人的神经系统。然而,磁共振成像已经表明,当一个人正在进行MS“攻击”时,血脑屏障在大脑或脊髓的一部分中已经破裂,允许称为T淋巴细胞的白细胞跨越并攻击髓鞘。有时有人提出,MS不是免疫系统的疾病,而是血脑屏障的疾病。[51]血脑屏障的减弱可能是血管内皮细胞紊乱的结果,因此蛋白质P-糖蛋白的产生效果不佳。[52]
目前正在积极研究血液屏障受损的治疗方法。据信氧化应激在屏障破坏中起重要作用。抗氧化剂如硫辛酸可能能够稳定弱化的血脑屏障。[53]
视神经脊髓炎
视神经脊髓炎,也称为Devic's病,与多发性硬化相似并且经常混淆。在与MS的其他差异中,已经鉴定了自身免疫应答的不同目标。视神经脊髓炎患者的抗体水平高,称为水通道蛋白4(血脑屏障中星形细胞足突的一个组成部分)。[54]
晚期神经系统锥虫病(昏睡病)
晚期神经性锥虫病或昏睡病是在脑组织中发现锥虫原生动物的病症。目前尚不清楚寄生虫如何从血液中感染大脑,但怀疑它们穿过脉络丛,即周围器官。
进行性多灶性白质脑病(PML)
进行性多灶性白质脑病(PML)是中枢神经系统的脱髓鞘疾病,其由可以穿过BBB的潜伏乳多空病毒(JC多瘤病毒)感染的再激活引起。它影响免疫受损的患者,通常见于患有艾滋病的患者。
De Vivo疾病
De Vivo疾病(也称为GLUT1缺乏综合征)是由于糖葡萄糖在血脑屏障上的运输不足引起的罕见病症,导致发育迟缓和其他神经学问题。葡萄糖转运蛋白1型(GLUT1)的遗传缺陷似乎是De Vivo疾病的主要原因[55][56]。
阿尔茨海默氏病
一些证据表明,阿尔茨海默病患者血脑屏障的破坏使得含有淀粉样蛋白β(Aβ)的血浆进入大脑,而Aβ优先附着在星形胶质细胞表面。[57]这些发现导致了以下假设:(1)血脑屏障的破坏允许神经元结合自身抗体和可溶性外源Aβ42进入脑神经元和(2)这些自身抗体与神经元的结合触发和/或促进内化和细胞表面结合的Aβ42通过内吞作用清除表面结合的自身抗体的自然倾向,在脆弱的神经元中积累。最终星形胶质细胞不堪重负,死亡,破裂和崩解,留下不溶的Aβ42斑块。因此,在一些患者中,阿尔茨海默病可能由于血脑屏障的破坏而引起(或更可能是加重)。[58]
脑水肿
脑水肿是大脑细胞外空间中多余水分的积累,当缺氧导致血脑屏障打开时,可导致脑水肿。
朊病毒和朊病毒样疾病
许多神经退行性疾病,包括帕金森病等突触核蛋白病,以及阿尔茨海默氏症等τ蛋白病,都被认为是由称为朊病毒的病理性细胞外蛋白变种的种子错误折叠引起的。这种类似朊病毒的假说在许多体外研究中得到了支持,并涉及脑内裂解物,提取蛋白(tau,α-突触核蛋白)和α-突触核蛋白病中合成产生的纤维的体内脑内注射。这些蛋白质在患有这些病症的患者的血浆中也可以检测到增加的量(特别是帕金森氏病患者中的总α-突触核蛋白)。目前还不知道这些朊病毒样蛋白质可以穿透血脑屏障的程度和机制。
艾滋病毒性脑炎
据信[59],潜伏的HIV可以在感染的前14天内穿过血流中循环单核细胞内的血脑屏障(“特洛伊木马理论”)。一旦进入,这些单核细胞就会被激活并转化为巨噬细胞。活化的巨噬细胞将病毒颗粒释放到靠近脑微血管的脑组织中。这些病毒颗粒可能引起前哨脑小胶质细胞和血管周围巨噬细胞的注意,引发炎症级联,可能在脑微血管内皮细胞中引起一系列细胞内信号传导,并破坏BBB的功能和结构完整性。[60]这种炎症是HIV脑炎(HIVE)。HIVE的实例可能在整个艾滋病过程中发生,并且是HIV相关性痴呆(HAD)的前兆。研究HIV和HIVE的首要模型是猿猴模型。
狂犬病
在致死性狂犬病感染小鼠期间,血脑屏障(BBB)不允许抗病毒免疫细胞进入大脑,这是狂犬病病毒复制的主要部位。该方面有助于病毒的致病性,并且人工增加BBB通透性促进病毒清除。尽管还没有尝试确定这种治疗方法是否成功,但在狂犬病感染期间打开BBB已被认为是治疗该疾病的一种新方法。[原创研究?]
全身性炎症
体内炎症可能通过血脑屏障导致对大脑的影响。在全身性炎症期间,无论是以感染形式还是无菌性炎症,BBB都可能发生可能具有破坏性或无破坏性的变化。[61]这些变化可能是对系统性炎症的有效宿主反应的一部分,或可能导致中枢神经系统内的有害后果。这些BBB变化可能在全身感染期间产生疾病行为中发挥作用。[引证需要]这些变化也可能诱发或加速大脑内的疾病,例如多发性硬化症和阿尔茨海默病,这可能是其中一部分原因。患有这些疾病的患者在感染期间会恶化。[62][63]此外,在患有神经疾病的患者中,BBB可能对全身性炎症的影响异常敏感。
历史
Paul Ehrlich是一位研究染色的细菌学家,这种方法在许多显微镜研究中用于使用化学染料制作精细的生物结构。[64]由于埃利希注射了一些这些染料(特别是当时广泛使用的苯胺染料),染料染色了某些动物的所有器官,除了它们的大脑。[64]那时,Ehrlich将这种缺乏染色的原因归结为大脑根本没有吸收尽可能多的染料。[65]
然而,在1913年的后期实验中,Edwin Goldmann(Ehrlich的学生之一)将染料直接注入动物脑的脑脊液中。然后他发现大脑确实染成了染色,但身体的其他部分却没有染色,证明两者之间存在分隔。那时,人们认为血管本身是造成屏障的原因,因为没有发现明显的膜。血脑屏障(当时称为血脑屏障)的概念是由柏林医生Lewandowsky在1900年提出的。[66]










