合作客户/
拜耳公司 |
同济大学 |
联合大学 |
美国保洁 |
美国强生 |
瑞士罗氏 |
相关新闻Info
推荐新闻Info
-
> 五种表面活性剂对粉煤灰基多孔地聚物孔结构与力学性能的调控机制(二)
> 五种表面活性剂对粉煤灰基多孔地聚物孔结构与力学性能的调控机制(一)
> 粉煤灰基多孔地聚物:五种表面活性剂降低碱液表面张力与稳定泡沫的效能对比
> 表面活性剂对粉煤灰基多孔地聚物孔结构及性能的调控机制研究
> 人工模拟瘤胃体外发酵技术:纤维发酵中比表面积与表面张力的调控作用(二)
> 人工模拟瘤胃体外发酵技术:纤维发酵中比表面积与表面张力的调控作用(一)
> 翅果油饮品加工工艺的创新与深度解析界面张力仪在其中的应用
> 基于界面张力最小化优化PS微球制备工艺:SDS与Na₂SO₄浓度的选择
> 表面张力降低视角下离子液体促进气体水合物生成的机理探究
> 低用量、高效率:离子液体促进剂实现水合物生成体系表面张力最大降低53.06%
细胞表面PH对于生物多肽生物活化的潜在重要性——摘要、介绍、材料和方法
来源:上海谓载 浏览 2523 次 发布时间:2022-01-04
摘要
细胞的糖酵解代谢产生质子,这些质子通过转运蛋白从细胞质中去除,从而在相邻的整体溶液和细胞膜表面之间产生pH差。因此,由于不同的糖萼和质子产生能力,组织细胞具有不同的表面pHs。在这项研究中,我们使用具有pH依赖活性的裂解肽作为探针,证明了细胞表面pH在肽-细胞相互作用和肽活化中的作用。适当地,所选择的肽能够感知细胞上特定的pH区域,因此对具有不同表面pH的组织细胞表现出不同的活性。对于特定的细胞,随着质子通道调节器调节细胞表面pH值的升高或降低,pH敏感肽的活性相应地发生变化。机理研究表明,细胞表面pH通过改变膜结合pH敏感肽的二级结构和聚集状态直接影响肽插入膜。根据正常-癌细胞对之间的细胞表面pH差设计的pH敏感裂解肽对癌细胞具有良好的选择性。因此,细胞表面pHs可能为设计具有高细胞特异性和选择性的治疗肽提供新的机会。
介绍
细胞的糖酵解代谢产生质子,这些质子通过转运蛋白(如Na+/H+交换异构体1(NHE1)(1,2))从细胞质中去除。在不限制质子扩散的情况下,喷射出的质子将在无限的外部溶液中被稀释。然而,哺乳动物细胞表面覆盖着一层致密的碳水化合物,由膜锚定糖蛋白和糖脂的共轭低聚糖链组成,称为糖萼(3)。由于这些带负电的大分子的存在,质子在膜-水界面上的扩散确实受到带负电膜表面水的低介电常数(e)的限制。因此,喷射出的质子很容易扩散到细胞膜表面,但不知何故无法迅速与体积平衡。据估计,该势垒可使膜表面的质子浓度比本体中的质子浓度高10-6 M,从而在细胞膜表面和相邻本体溶液之间产生pH差(4,5)。理论上,细胞表面的特定pH区可以通过影响细胞表面电荷、细胞表面的离子积累、细胞膜电位、药物吸收以及肽/蛋白质与受体的结合对细胞产生重大影响。不幸的是,细胞表面pHs的生物学重要性和潜在的药学意义被忽视了。
我们知道,肽转变为结合平面和插入细胞膜是生物活性肽发挥其生物活性的关键步骤(6)。在本研究中,选择一组具有pH依赖性细胞裂解活性的裂解肽(pH敏感裂解肽)作为探针,通过检测细胞表面pHs影响的肽-细胞相互作用和肽活化来评估细胞表面pHs的药学意义。
方法和材料
材料
肽(纯度>90%)由Genescript公司(美国新泽西州皮斯卡塔韦)合成。将肽溶解在含有10%二甲基亚砜(DMSO)的水中,形成5.0 mM储备溶液。使用合适的细胞培养基,从储备溶液中逐渐稀释制备肽工作溶液。活/死细菌染色试剂盒购自Invitrogen Life Technologies(美国加利福尼亚州卡尔斯巴德)。所有其他化学品均从Sigma-Aldrich Co.(美国密苏里州圣路易斯)购买。
细胞培养
所有细胞均取自美国类型培养物收集中心(ATCC)。A549和CHO-K1细胞在F12K中生长,NIH/3T3细胞在DMEM中生长,CCD-Lu13细胞在MEM中生长。所有培养基均添加10%胎牛血清(FBS)。细胞在37°C、5%CO2的增湿空气中培养。
肽的pH敏感性
如前所述(6),在负载钙黄绿素的大单膜囊泡(LUV)上测试肽的裂解活性。通过将激发和发射波长分别设置为485和530 nm,使用荧光微孔板读取器监测肽诱导的钙黄绿素泄漏(通过荧光强度的增加反映)。从LUV释放的钙黄绿素表示为F/F0,其中F0和F分别表示在不存在和存在肽的情况下负载钙黄绿素的LUV的荧光强度。已经证明,pH敏感裂解肽的活性变化通常发生在狭窄的pH范围内,即所谓的肽转变pH值,即当肽的净电荷为零(6)时的pH值,如图1所示。使用纳米试剂(6)测定肽的过渡pH值。简单地说,用不同pH值(pH=5.0–9.0)的PBS稀释来自储备溶液(水中5mM)的肽。对新制备的肽溶液(40 lM)进行短暂(60秒)的超声处理。使用zeta纳米分析仪在超声处理后立即测量肽溶液的zeta电位。
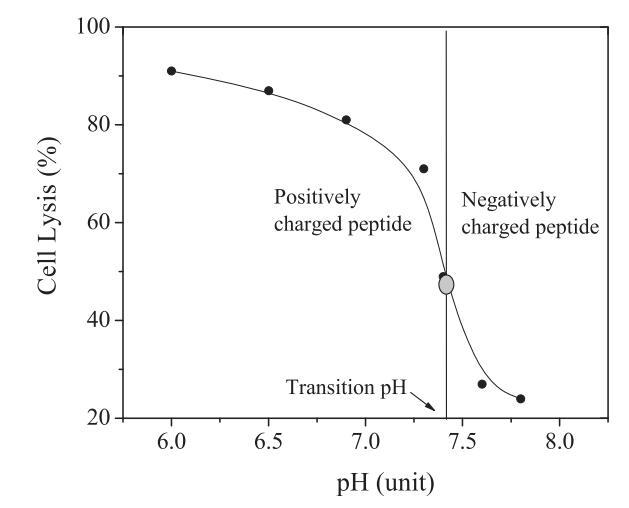
图1:过渡pH=7.35的肽CL-7的pH依赖性膜裂解活性。
细胞表面pHs的测量
共有2.59105个细胞接种在胶原涂层的覆盖玻璃上并培养过夜。细胞在无血清培养基中用荧光素结合麦胚凝集素(WGA)(12.5 lM)染色30 min,然后将盖玻璃组装到FCS2流动室系统(BioTechs Inc.,Butler,PA,USA)。使用视频成像技术测量pH值。将盖玻璃置于共焦显微镜(LSM510;美国纽约桑伍德卡尔蔡司有限公司)的台上,并以0.1ml/min的速度连续超灌注预热(37°C)Hepes缓冲林格溶液(122.5mmNaCl、5.4mmKCl、0.8mmMgCl2、1.2mmCaCl2、1.0mmNaH2PO4·2H2O、5.0mm葡萄糖、10mmHEPES;pH=7.4)波长在458和488 nm之间交替,而发射的荧光强度记录在560 nm以上。根据在458和488 nm处测得的发射荧光强度计算出比率。因此,该测量实际上与给定感兴趣区域中激发的染料量无关,并表示局部质子浓度(1)。以1.0秒的间隔测量荧光强度,平均测量10次,并通过减去位于测量的感兴趣区域旁边的对照区域的背景强度来校正背景荧光。在每个实验结束时,通过使用不同pH值(pH=8.5、8.0、7.4、7.0、6.5和6.0)的改良Ringer溶液(125 mM KCl、1 mM MgCl2、1 mM CaCl2、20 mM Hepes和10 mM nigericin)连续超滤池,校准pH测量值。荧光素在6-10的pH范围内具有良好的荧光强度-pH相关性。
细胞表面电荷的测定
将细胞接种于浓度为5 9 104个细胞/mL的细胞培养瓶中。培养48小时后,从培养瓶中刮下细胞,用PBS洗涤,并在0.25 M蔗糖溶液中重新悬浮至最终浓度为106个细胞/mL。然后用1%甲苯胺蓝染色细胞悬浮液90分钟。之后,用聚1,1-二甲基-3,5-二甲基哌啶氯化铵(CFC)溶液滴定细胞。根据先前出版物(7)中描述的程序,通过将总电荷与电池数量归一化来计算电池表面电荷。
肽圆二色光谱的获取
肽的圆二色谱(CD)光谱记录在Jasco J-710分光旋光仪上(Jasco公司,美国马里兰州伊斯顿)(6)。在25°C条件下,在光程长度为1.0-mm的带帽石英光学池中扫描CD光谱。以1.0 nm的间隔从250至190 nm收集数据,每个波长的积分时间为2秒。对每次测量的五到十次扫描进行平均、平滑、背景减去,并转换为平均残余摩尔椭圆度[h](度cm2 dmol?1)。CDPRO软件用于分析从CD分光旋光仪获得的数据。
肽诱导细胞裂解的测定
在暴露于肽之前,在96孔板(5 9 103个细胞/孔)上过夜培养的细胞用PBS洗涤三次。在孵育60分钟后,通过使用乳酸脱氢酶试剂盒测量受损细胞的乳酸脱氢酶(LDH)释放,定量评估肽诱导的细胞膜损伤。通过将参考波长设置为690 nm,使用微孔板读取器(美国VT威努斯基Biotek Inc.)测量490 nm处的吸光度。对照空白对照组和100%裂解对照组,结果均标准化为细胞死亡百分比。
肽诱导细胞膜损伤的动力学
将新鲜胰蛋白酶化的人肺癌A549细胞接种于胶原涂层的八孔玻璃室内(2 9 104个细胞/孔),并培养过夜。试验前,用PBS清洗细胞三次,并用活/死染色试剂盒染色15分钟。添加肽后,使用蔡司LSM510共焦显微镜(卡尔蔡司公司)在不同时间点记录细胞图像。激发波长固定在488 nm,发射波长分别设置为505–530 nm(活细胞)和560 nm(死细胞)。计算捕获的细胞图像中绿色像素占总绿色和红色像素的百分比,以估计细胞膜完整性(8)。
肽与脂膜的相互作用
使用组装在微槽X上的脂质单层研究肽与细胞膜的相互作用(芬兰赫尔辛基Kibron公司)(6)。将DPPC/胆固醇/DPPS(50/10/2.5)的脂质混合物溶解在3:1氯仿:甲醇中,形成100 lM脂质溶液。向四孔聚四氟乙烯板中添加1.0 mL PBS,然后滴一滴脂质溶液。有机溶剂蒸发后,在水面形成脂质单层。通过特氟隆板的侧孔将肽溶液添加到亚相后,立即记录肽诱导的表面张力变化。
pH敏感肽对正常细胞和癌细胞的毒性
使用MTT[3-(4,5-二甲基噻唑-2-基)-2,5-二苯基四唑溴化盐]分析,在癌-正常对(A549和CCD-13Lu)上比较pH敏感和pH不敏感裂解肽对正常和癌细胞的细胞毒性。简而言之,将完整培养基中的细胞加入96孔板(5 9 103个细胞/孔)中,并在37°C下培养14–16小时。洗涤后,用含有不同浓度肽的无血清培养基喂养细胞,并在37°C下培养2小时。之后,向每个孔中加入10 lL MTT(5 mg/mL)。培养4小时后,通过用含有5%异丙醇和0.1%HCl的10%SDS溶液溶解福尔马赞并在570 nm(9)处测量吸光度来测定细胞活力。
肽在溶液中的自组装和聚集特性
使用荧光探针1-苯胺基萘-8-磺酸(1,8-ANS)(6,10)估计肽在溶液中自组装形成肽聚集体。通过将激发波长设置为369 nm,在荧光微孔板阅读器(Biotek Inc.)上记录了460–500 nm处由肽聚集引起的1,8-ANS(20 lM)荧光发射光谱增加。
使用zeta纳米分析仪测量肽溶液在不同pH下的粒径和zeta电位变化。在每次测量之前,肽溶液经过短暂(60秒)的超声处理。
利用扫描电子显微镜(SEM)研究了肽聚集体的形态。将肽溶液装载到硅片上并孵育30分钟。用去离子水洗涤后,硅片上的肽样品涂上金。使用Auriga模块化横梁工作站(卡尔蔡司公司)获取SEM图像。










