合作客户/
拜耳公司 |
同济大学 |
联合大学 |
美国保洁 |
美国强生 |
瑞士罗氏 |
相关新闻Info
推荐新闻Info
-
> 超微量天平在药物研发中的应用:精确称量活性成分与标准品
> 超微量天平工作原理,如何为药物研发实验室选择超微量天平?
> 醇醚硫酸盐泡排剂的耐温耐盐性能及分子机理研究
> 利用表/界面张力仪评价醇醚硫酸盐耐凝析油泡沫排液性能
> mRNA疫苗开发关键:脂质纳米粒(LNP)表面张力精准调控方案
> PAAS/CA/SSD双网络水凝胶制备及表面张力调控研究(三)
> PAAS/CA/SSD双网络水凝胶制备及表面张力调控研究(二)
> PAAS/CA/SSD双网络水凝胶制备及表面张力调控研究(一)
> 从无序到有序:双乳液模板如何重塑中空材料合成与电池未来
> 微乳液:以超低界面张力撬动老油田残余油的核心技术
首次揭示溶酶体修复的核心机制,理解衰老更近一步
来源:转化医学网 浏览 1981 次 发布时间:2022-09-13
导读:近几十年来,已有诸多研究发现了溶酶体的重要功能——参与细胞免疫、营养感知、清除受损细胞组分、降解生物大分子等诸多细胞活动。因此,溶酶体本身的损伤及活性下降,在衰老和疾病中扮演着重要角色;但一直以来鲜有研究对溶酶体的修复机制进行深入探索。近日,科学家们首次揭示了溶酶体修复的核心机制——该机制将引领人们进一步探索众多与衰老相关的疾病,尤其是包括阿尔茨海默病在内的神经退性疾病。
9月7日,来自匹兹堡大学医学院细胞生物学系的谭小军博士与衰老研究所所长Toren Finkel博士在《自然》(Nature)杂志发表了一篇题为“A phosphoinositide signalling pathway mediates rapid lysosomal repair”的细胞生物学领域研究论文。研究者们通过一系列实验,首次描述了一种溶酶体修复的核心途径:PITT途径(phosphoinositide-initiated membrane tethering and lipid transport)。通过该途径,细胞能快速修复已受损的溶酶体。该发现将协助人们进一步了解和治疗由溶酶体受损驱动的与年龄相关的疾病。

https://www.nature.com/articles/s41586-022-05164-4
细胞的“自杀口袋”——溶酶体
01
20世纪50年代,现代细胞生物学创始人之一、诺贝尔生理学或医学奖得主Christian de Duve教授首次发现了动物细胞中的“溶酶体”(lysosomes),并且一度称之为细胞的“自杀口袋”:这种细胞器含有大量水解酶,可降解细胞内的蛋白质等生物大分子;由此可能在细胞自杀过程中发挥作用。随着近几十年来对溶酶体的进一步探索,人们已发现溶酶体的诸多其他重要功能——例如,参与细胞免疫、营养感知、清除受损细胞组分等细胞活动。由此,溶酶体自身的损伤及活性下降,在细胞衰老、人类疾病中扮演着至关重要的角色。
该研究论文的第一作者、来自匹兹堡大学医学院的谭小军博士表示:“溶酶体损伤是包括衰老在内的许多疾病的标志,尤其像阿尔茨海默病等神经退行性疾病。探索、理解溶酶体修复的核心机制,将帮助我们进一步研究正常衰老、与衰老相关的疾病。”
溶酶体修复核心机制——PITT途径
02
之前的研究普遍认为,细胞中存在两种潜在的溶酶体修复机制——溶酶体自噬(lysophagy)介导的间接修复;以及内体分选复合物(ESCRT)介导的直接膜孔修复。然而,科学家发现,在缺乏上述两种机制的情况下,溶酶体损伤仍然能够被快速修复;这不禁让人猜测,细胞中还存在更重要的修复途径来治愈溶酶体损伤。
首先,研究者用生物素对溶酶体表面的所有蛋白进行了标记,然后通过组学方法来寻找溶酶体受损后,表面特异性富集的蛋白。此研究发现,溶酶体一旦受损,在短短几分钟后,一种叫PI4K2A的激酶就会到达现场,随后导致脂质信号PI4P(磷脂酰肌醇4-磷酸)大量富集于溶酶体表面。
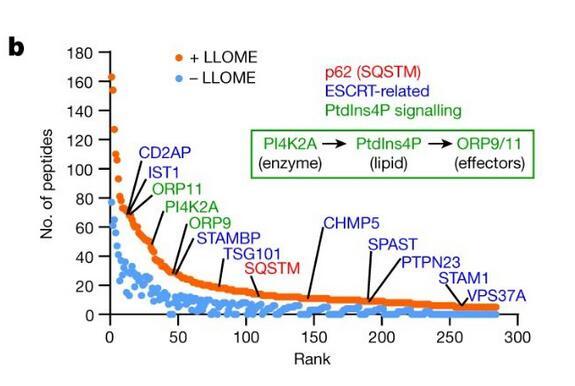
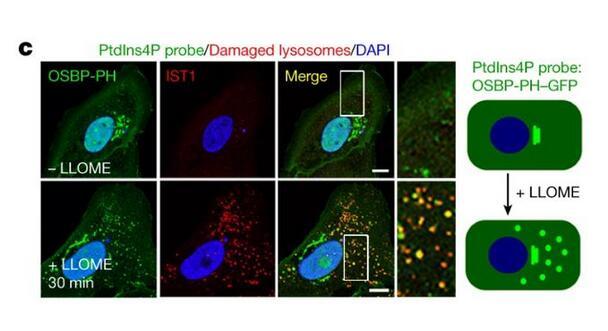
蛋白组学揭示受损溶酶体表面的PI4P信号:
b.蛋白组学分析溶酶体表面蛋白;
c.受损溶酶体PI4P信号示意图。
PI4P信号触发了“警报系统”,有选择性地对受损溶酶体进行标记。这将进一步招募ORP家族蛋白(包括ORP9/10/11和OSBP)——它们一端结合受损溶酶体上的PI4P,另一端结合在内质网上。内质网是细胞中最大的膜结构细胞器,负责脂质与蛋白质的合成。在ORP家族蛋白的帮助下,内质网与受损溶酶体紧密地结合起来。
在一般的情况下,内质网和溶酶体几乎不会接触,或者仅有十分短暂的局部接触;但此研究发现,一旦溶酶体受损,内质网和溶酶体就会“相互拥抱”。谭小军博士表示,这可能是目前观察到的最强的细胞器间互作。
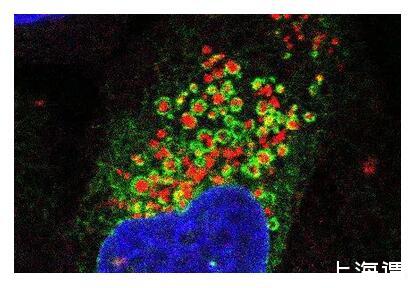
荧光显微图像显示了内质网(绿色)像毯子一样包裹住受损的溶酶体(红色),细胞核以蓝色显示。
通过这种“拥抱”,ORP家族蛋白作为脂质转运体,继而将胆固醇和一种叫做磷脂酰丝氨酸(PS)的脂质从内质网运送到溶酶体,以促进溶酶体膜的修复。研究者发现,只要溶酶体上能富集胆固醇和PS中的一种,受损溶酶体就能得到快速修复。胆固醇含量上升可以提高细胞膜的稳定性,这可能预示胆固醇或许直接参与溶酶体修复。然而,PS并没有已知的提高生物膜稳定性的功能。为了破解PS如何介导溶酶体修复,研究者们将目光投向了一系列可能被PS激活的大规模脂质转运蛋白。
他们发现,溶酶体上的PS激活了一种被称为ATG2的脂质转运蛋白。ATG2就像一座桥梁,将大量脂质运送到溶酶体,直接修复溶酶体膜,在新发现的这一修复途径中完成最后一步。
研究者表示:“ATG2有一个经典的功能,即转运脂质介导自噬体的形成。自噬和溶酶体修复都依赖于ATG2的脂质转运功能,但两个过程相互独立,互不影响。”通过在溶酶体表面过表达ATG2的一个片段,研究人员选择性地阻断了内源性ATG2介导的溶酶体修复,发现ATG2在自噬中的作用并未受此影响。
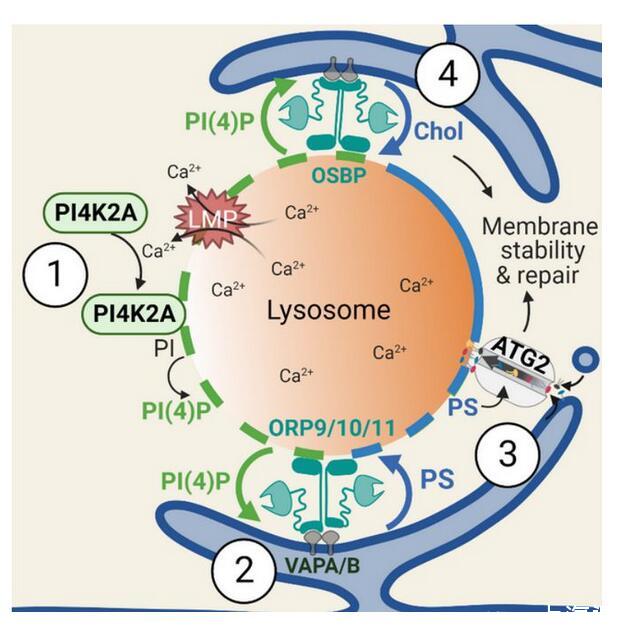
细胞快速修复溶酶体损伤的统一核心机制:PITT途径
对理解衰老、衰老相关疾病的意义
03
综上,此研究发现了细胞快速修复溶酶体损伤的核心机制——溶酶体损伤促发了溶酶体表面的一种特殊脂质信号PI4P;而这一信号推动了内质网和溶酶体间的强烈互作,进而激活内质网向溶酶体的多重脂质转运。
Finkel博士说表示:“这个系统的美妙之处在于,PITT途径的所有参与蛋白都是已知的分子,但过去并不知道它们会相互合作以及在溶酶体修复过程中发挥作用。这些发现将对理解正常衰老和与衰老相关的疾病产生重要意义。”
作者发现,多种不同机制导致的溶酶体损伤,都能激活PITT途径。由此推测,在健康人体内,溶酶体膜的小破损会通过PITT途径迅速得到修复。然而,当损伤过度时——由于衰老或疾病等因素导致修复途径受阻,破损的溶酶体会积聚在细胞内导致二次伤害。
以阿尔茨海默病为例,tau纤维突破溶酶体膜继而侵袭扩散是疾病进展的关键步骤。此研究通过实验敲除了编码PITT途径中第一个酶PI4K2A的基因,发现tau纤维的侵袭扩散急剧增加,这表明PITT途径的缺陷可能加速阿尔茨海默病的进程。
在未来,研究者计划开发小鼠模型,以了解激活PITT途径能否保护小鼠免于患上阿尔茨海默病的发展。
参考资料:
https://phys.org/news/2022-09-pitt-pathway-scientists-cells-longevity-promoting.html
http://k.sina.com.cn/article_5895622040_15f680d9802001dr6m.html?display=0&retcode=0
注:本文旨在介绍医学研究进展,不能作为治疗方案参考。如需获得健康指导,请至正规医院就诊。










