合作客户/
拜耳公司 |
同济大学 |
联合大学 |
美国保洁 |
美国强生 |
瑞士罗氏 |
相关新闻Info
-
> 植物油中N-酰基氨基酸表面活性剂的界面活性和聚集行为——材料和方法
> 起泡和去污的关键成分——表面活性剂
> 改变表面张力的plasma等离子清洗机有什么作用?
> 水和乙二醇-水混合体系中的离子液体-阳离子表面活性剂混合胶束自聚焦-电导法 表面张立法和光谱研究法—
> 中性墨水技术研发所面临的主要技术难题
> 采用壳聚糖-三聚磷酸酯-百里香纳米颗粒经热喷墨打印而成的新型活性包装材料——摘要、简介
> 液体与大气之间的界面,液体与固体之间界面,它们与其它部位有什么不同?为什么这里会出现所谓张力?
> 微尺度区域内静电相互作用力动态调节和脂质双分子层的分布——结论、致谢!
> 三防漆产生毛细现象的原因及解决方案
> 生物降解过程中对于表面活性剂AS、AE的表面活性以及水生生物毒性的性能的关系——结论、致谢!
推荐新闻Info
-
> 界面张力仪的关键证据:量化润湿性变化阐明改性碳烟润滑增效机制
> 从界面张力到摩擦性能:改性生物柴油碳烟作为水基润滑添加剂的构效关系分析
> 芬兰Kibron SuperG超微量天平技术参数详解与选购指南
> 五种表面活性剂对粉煤灰基多孔地聚物孔结构与力学性能的调控机制(二)
> 五种表面活性剂对粉煤灰基多孔地聚物孔结构与力学性能的调控机制(一)
> 粉煤灰基多孔地聚物:五种表面活性剂降低碱液表面张力与稳定泡沫的效能对比
> 表面活性剂对粉煤灰基多孔地聚物孔结构及性能的调控机制研究
> 人工模拟瘤胃体外发酵技术:纤维发酵中比表面积与表面张力的调控作用(二)
> 人工模拟瘤胃体外发酵技术:纤维发酵中比表面积与表面张力的调控作用(一)
> 翅果油饮品加工工艺的创新与深度解析界面张力仪在其中的应用
海洋细菌中生物表面活性物质——结果和讨论
来源:上海谓载 浏览 2124 次 发布时间:2021-10-19
结果和讨论
筛选 SAC 生产商
SAC 生产的筛选包括 84 种新的烃降解分离株和 93 株来自挪威渔业科学学院 (NCFS) 的培养物保藏中心。 所有分离株均在补充有 1% 葡萄糖或煤油作为唯一碳源的 MBH 培养基中筛选。 在测试的所有分离株中,100 个分离株在至少一项定性筛选试验(光学变形、油扩散或乳化试验)中显示出阳性结果。
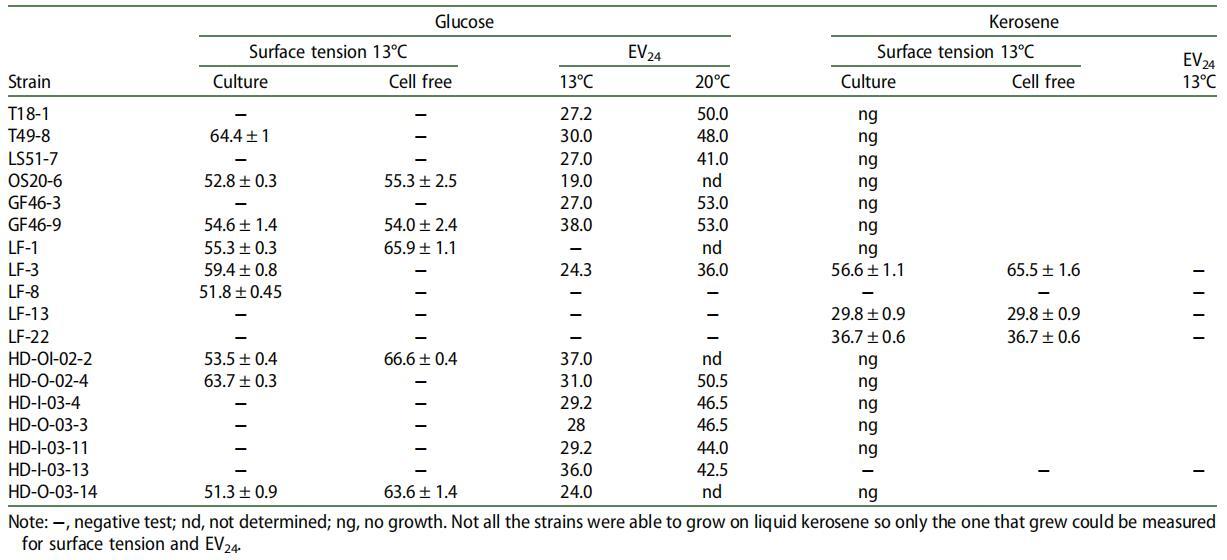
对于 SAC 生产的定量评估,确定了表面张力和乳化活性。 良好的生物表面活性剂应能够将水或培养基的表面张力降低 ≥20 mN m-1 [13] 或 ≥40 mN m-1。[18] 良好的生物乳化剂的 EV24 值应高于 50%。 19] 在 100 个阳性分离株中,只有 4 个菌株能够将培养基的表面张力从 72 mN m-1 的未接种培养基降低至少 20 mN m-1(表 1)。 没有一株分离株的 EV24 值高于 50%,但其中 18 株的 EV24 值≥19%(表 1)。 我们研究中的培养温度为 13°C,低于之前研究中使用的温度(28°C),[14,20] 可能影响了受试菌株的乳化活性。 因此,在 13°C 下 EV24 值≥20% 的分离株在 20°C 下培养。 结果证实,较低的生长温度导致测试培养物的较低乳化活性。 11 个分离株中有 10 个在 20°C 下显示出 EV24 >40%(表 1)。
表 1. 在葡萄糖和煤油上生长的细菌菌株的培养物和培养物滤液的表面张力和乳化值。
16S rRNA基因测序分析
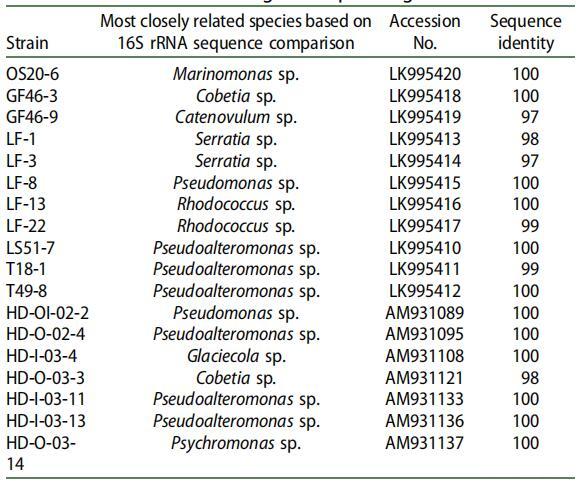
通过 16S rRNA 基因序列分析对具有显着 SAC 活性的 18 个分离株进行分类鉴定(表 2)。 红球菌除外。 菌株 LF-13 和红球菌属。 在菌株 LF-22 中,大多数鉴定的 SAC 生产者是革兰氏阴性菌,属于 γ-变形菌纲。 也有报道称 γ-变形菌在寒冷海洋地区的石油污染地点占优势。 [21-24] 先前对石油污染地点的研究表明,假单胞菌、假交替单胞菌、冰川、海藻和红球菌是极地、海洋区域。[21,22,25-28]
表 2. 选定的 SAC 产生的分类从属关系 基于 16S rRNA 基因测序的细菌。
已对假单胞菌属的代表产生鼠李糖脂 [29,30] 和脂肽 [31-33] 和其他高分子量生物乳化剂的能力进行了深入研究。 [34,35] 红球菌属以其产生鼠李糖脂的能力而闻名。 [36-38] 具有 SAC 活性的胞外多糖 (EPS) 已被证明是由从海洋环境中分离出来的假交替单胞菌属的几个成员分泌的。[39-42] 耐冷假交替单胞菌属。 从海冰样品中分离出的菌株 CAM025 在 -2 和 10°C 下的 EPS 产量是 20°C 下的 30 倍。 [41] 松山等人。 [43] 描述了两种菌株 Glaciecola chathamensis 的 S18K6T 和 S18K5 菌株产生 EPS 的能力。 据我们所知,迄今为止,尚未确定 Psychromonas 和 Marinomonas 属的成员能够产生 SAC。 因此,目前的分离株是产生 SAC 的分类群列表的补充。
生物表面活性剂生产
基质
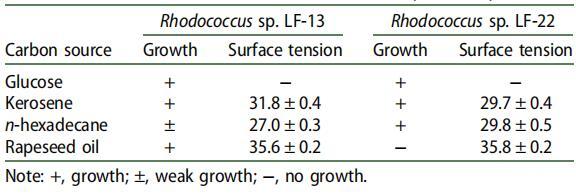
两种细菌菌株红球菌属。 菌株 LF-13 和红球菌属。 当以煤油作为唯一碳源和能源时,菌株 LF-22 能够将培养基的表面张力降低约 40 mN m-1。 因此,它们被选择用于进一步表征生物表面活性剂的生产。 为了拓宽生物表面活性剂生产的底物范围,测试了除煤油和葡萄糖之外的其他碳源(表 3)。 这两种菌株可以在葡萄糖上生长,但不合成生物表面活性剂。 他们能够在正十六烷和菜籽油上产生 SAC,即使菜籽油不支持菌株 LF-22 的生长。
表 3. 所选培养物中的生长和表面张力 不同碳源上的细菌分离物 (1% w/w)。
生长细胞的生物表面活性剂生产
菌株红球菌属。 菌株 LF-13 和红球菌属。 大约 2 天后,菌株 LF-22 达到稳定期(图 1)。 LF-13 和 LF-22 的培养物表面张力的最低值分别为 31.8 和 29.3 mN m-1,当培养物达到稳定期时(图 1)。 无细胞制剂的值显示出与培养物类似的降低,表明生物表面活性剂被释放到培养基中。 从工业角度来看,将生物表面活性剂分泌到培养基中的分离物很有趣,因为这使得生物表面活性剂的纯化过程更简单。 [16,44,45]
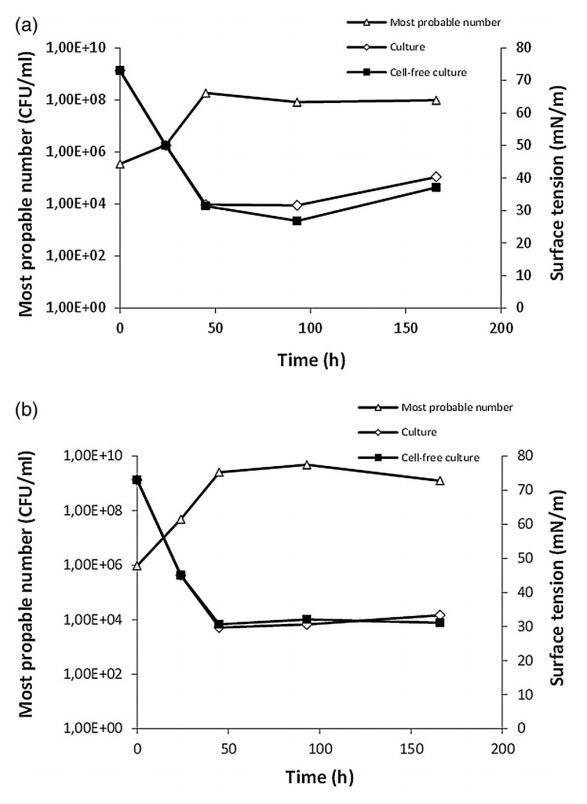
图 1. (A) 红球菌属的生长曲线和表面张力降低曲线。 菌株LF-13; (B) 红球菌属。 菌株LF-22; 在以 2% 煤油为碳源的 MBH 中培养,20°C,160 rpm。 结果代表三个独立实验的平均值。
静息细胞产生生物表面活性剂
为了确定生物表面活性剂的合成是否与石油烃上的细菌生长有关,在磷酸盐缓冲液和煤油中对两种菌株 LF-13 和 LF-22 进行了静息细胞实验。 红球菌属的细胞悬液和无细胞培养滤液的表面张力。 LF-13 和红球菌属。 LF-22 静息细胞在培养 2 天后显示出显着减少,从 72 到 26 mN m-1(图 2)。 结果表明,红球菌菌株中的生物表面活性剂合成发生在煤油存在下,但不一定与煤油上的细菌生长有关。
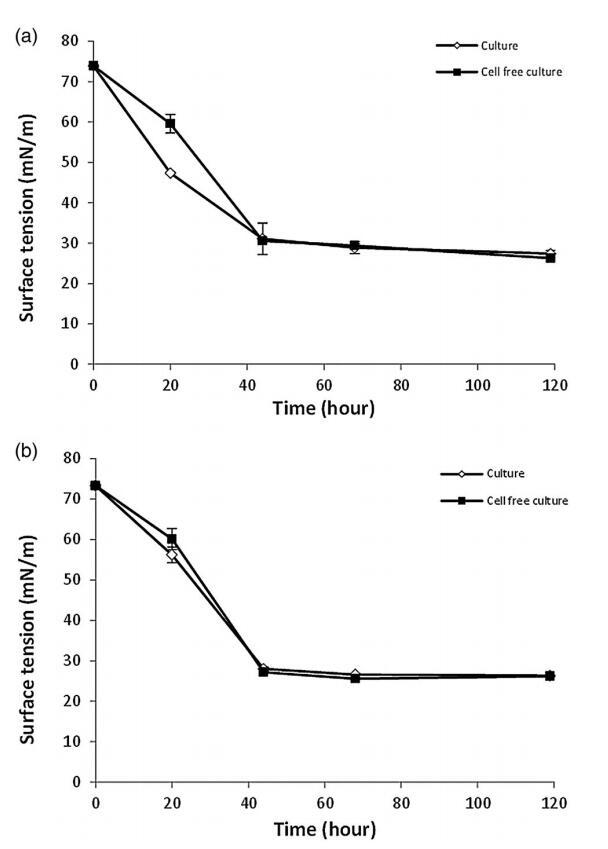
图 2. (A) 红球菌属的表面张力降低。 菌株LF-13; (B):红球菌属。 LF-22 菌株,在静息细胞条件下,含 2% (w/w) 煤油,有限氮源,20°C 和 160 rpm。 结果代表三个独立实验的平均值。
生物表面活性剂粗提物的产量约为 1.2–1.5 g/g 干燥静息细胞。 对于红球菌 erythropolis 菌株 DSM 43215 [46] 和菌株 SD-74 [36],已经建议通过静息细胞以比生长细胞更高的产量生产生物表面活性剂。 根据 Kitamoto 等人的建议,使用南极假丝酵母的静息细胞连续生产甘露糖赤藓糖醇脂质。 [47] 估计与生长细胞的生产相比具有更低的成本。
粗生物表面活性剂的CMC
如材料和方法部分所述,使用 MTBE 从两种红球菌属菌株的静息细胞培养物中提取生物表面活性剂。 提取的生物表面活性剂用于测定CMC浓度。 来自菌株 LF-13 的生物表面活性剂的 CMC 约为 217 mg/L,菌株 LF-22 的 CMC 约为 269 mg/L(图 3)。
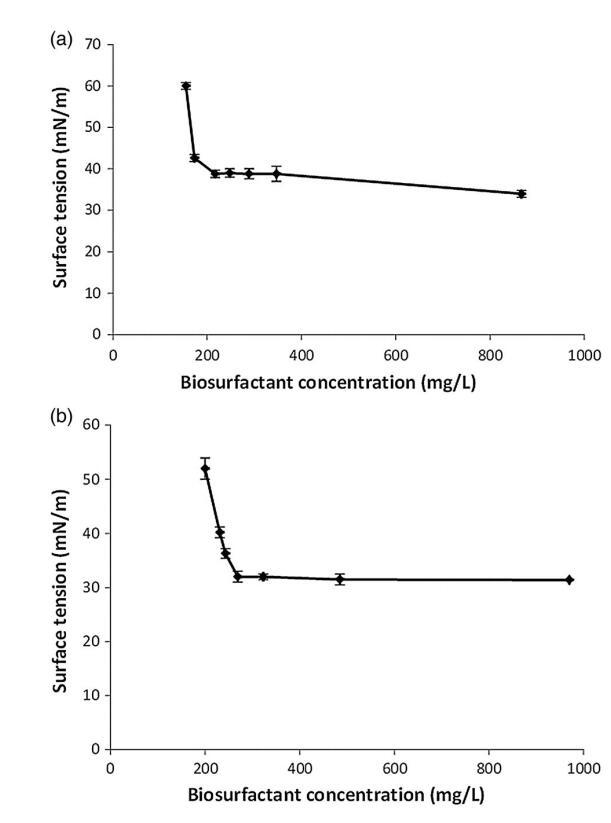
图 3. 从红球菌属静止细胞中提取的 SAC 的 CMC。 LF-13 和红球菌属。 LF-22。
增强正十六烷的生物降解
样品 2,仅包含含有正十六烷和来自红球菌属的生物表面活性剂的海水。 LF-22 没有显示出光密度 (OD) 的任何增加。 在 13°C 孵育 17 天后,样品中正十六烷的量为初始量的 78.4%,略低于对照样品(样品 1)的 86.5%(表 4)。 由于海水经过高压灭菌,我们预计样品 2 中的正十六烷不会发生任何生物降解。实验期间表面张力没有变化,表明添加的生物表面活性剂在海水中保持完整。
表 4. 正十六烷生物降解试验中的细菌生长、表面张力和正十六烷残留量(结果为两次重复的平均值)。
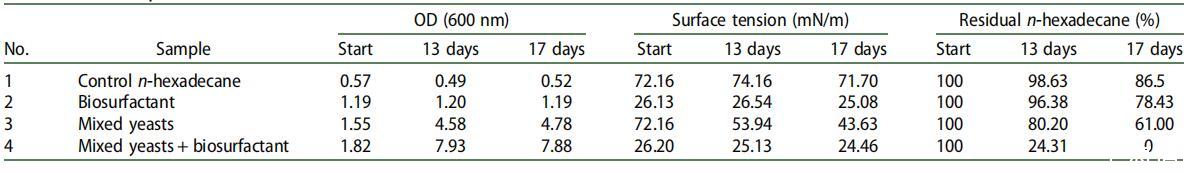
用耶氏酵母的混合培养物 LS-DO 修正的样品 3 显示测得的 OD 增加了约 3 倍,表明酵母在正十六烷上生长。 17 天后,样品中残留的正十六烷含量为 61%(表 4)。
用酵母和生物表面活性剂修饰的样品 4 表现出最高的 OD 增加,即与起始值相比增加了 4.4 倍,表明酵母在生物表面活性剂存在下生长得更快(表 4)。 正十六烷的降解率从用酵母修正时的 12 毫克/天增加到酵母和生物表面活性剂同时存在时的 30 毫克/天。 在生物表面活性剂存在下 17 天后,正十六烷耗尽。










