合作客户/
拜耳公司 |
同济大学 |
联合大学 |
美国保洁 |
美国强生 |
瑞士罗氏 |
相关新闻Info
推荐新闻Info
-
> 粉煤灰基多孔地聚物:五种表面活性剂降低碱液表面张力与稳定泡沫的效能对比
> 表面活性剂对粉煤灰基多孔地聚物孔结构及性能的调控机制研究
> 人工模拟瘤胃体外发酵技术:纤维发酵中比表面积与表面张力的调控作用(二)
> 人工模拟瘤胃体外发酵技术:纤维发酵中比表面积与表面张力的调控作用(一)
> 翅果油饮品加工工艺的创新与深度解析界面张力仪在其中的应用
> 基于界面张力最小化优化PS微球制备工艺:SDS与Na₂SO₄浓度的选择
> 表面张力降低视角下离子液体促进气体水合物生成的机理探究
> 低用量、高效率:离子液体促进剂实现水合物生成体系表面张力最大降低53.06%
> 离子液体促进剂显著降低气体水合物生成液的表面张力与表面能研究
> 表面张力怎么测?表面张力仪工作原理与校准全解析
新型注射剂之脂肪乳、纳米乳和脂质体
来源:药物递送 言成蹊 浏览 6322 次 发布时间:2022-09-15
传统注射剂在临床中广泛使用,但同时也暴露出不少问题,例如使用风险高、用药不便、药效维持时间短、患者依从性低等,因为使得新型注射剂成为新的临床需求。近些年,脂质体注射剂、混悬注射剂、微乳注射剂、纳米粒注射剂、微球注射剂、凝胶注射剂以及包合物注射剂等新型注射给药系统的开发,实现药物的缓控释,减少给药频次、提高药物疗效、降低毒副作用。
1、脂肪乳注射剂脂肪乳剂(Fat emulsions)又称为脂质乳剂(Lipid emulsions)或亚微乳(Submicron emulsions),是以植物油作为油相,辅以磷脂为主要乳化剂,甘油为等渗调节剂,经乳化制得的粒径在100~600 nm的水包油(O/W)乳剂微粒给药系统。一般而言,乳滴微粒中不含药的脂肪乳剂常用做肠外营养剂,而载药脂肪乳剂则作为药物载体使用。
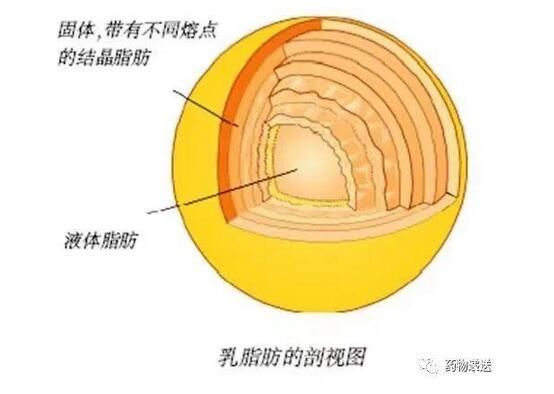
图1脂肪乳的结构第一个即用型营养脂肪乳Intralipid于1961年实现工业化生产并在瑞典上市,此后,营养型脂肪乳随着油相的改变不断地发展,主要变化为油相从单纯的大豆油改为中链油、橄榄油、鱼油以及多种油的混合物。营养型脂肪乳成功上市以后,医药行业在20世纪70年代将其应用作为难溶性药物静脉注射的载体,即载药脂肪乳剂。载药型脂肪乳除活性成分外,其处方组成与营养型脂肪乳基本一致。地塞米松棕榈酸酯和前列地尔脂肪乳剂于1988年上市,随后开发了多种载药脂肪乳剂,例如地西洋、丙泊酚、依托咪酯、氟比洛芬酯、氯维地平、阿瑞匹坦。表1已上市的部分营养乳商品名油相乳化剂其他成分Intralipid大豆油蛋黄卵磷脂甘油Abbolipid大豆油/红花油蛋黄卵磷脂甘油Deltalipid大豆油蛋黄卵磷脂/油酸甘油Salvilipid大豆油蛋黄卵磷脂/油酸钠甘油LipofundinN大豆油蛋黄卵磷脂/油酸钠甘油,生育酚Lipofundin MCT大豆油/中链油蛋黄卵磷脂/油酸钠甘油,生育酚Lipovenoes PLR大豆油蛋黄卵磷脂/油酸钠甘油Lipovenoes MCT大豆油/中链油蛋黄卵磷脂/油酸钠甘油橄榄油脂肪乳橄榄油蛋黄卵磷脂氨基酸、葡萄糖ω-3鱼油脂肪乳鱼油蛋黄卵磷脂甘油ω-3鱼油中/长链脂肪乳鱼油/中链油蛋黄卵磷脂甘油表2已上市的部分载药脂肪乳商品名药物油乳化剂国外上市国产化Liple前列地尔大豆油PC/油酸1988(日本)1998Limethason地塞米松棕榈酸酯大豆油蛋黄卵磷脂1988(日本)2010Diprivan丙泊酚大豆油蛋黄卵磷脂1989(美国)1999Lipo-NSAID氟比洛芬酯大豆油蛋黄卵磷脂1992(日本)2004Etomidaat-Lipuro依托咪酯大豆油/MCT蛋黄卵磷脂/油酸钠2001(德国)2002Diazepam-Lipuro地西泮大豆油/MCT蛋黄卵磷脂/油酸钠(欧洲)-VitalipideVit A,D2,E,K1大豆油蛋黄卵磷脂(欧洲)2005Propofol MCT丙泊酚大豆油/MCT蛋黄卵磷脂/油酸2005(欧洲)2013Cleviprex丁酸氯维地平大豆油蛋黄卵磷脂/油酸2008(美国)-ALYPROST前列地尔大豆油PC/PG2013(日本)-Cinvanti阿瑞匹坦大豆油蛋黄卵磷脂/油酸钠2017(美国)-2、注射用纳米乳剂纳米乳中助乳化剂的加入能显著降低油、水两相界面的表面张力,仅需利用搅拌、超声、均质等简单方法即可制备出粒度分布均匀的纳米乳。但目前上市的纳米乳产品很少,主要受限于如下几点:(1)制备粒径为10~100nm的纳米乳需要更高浓度的乳化剂,过多的乳化剂会刺激注射部位;(2)纳米乳不耐稀释,如果水相过多则会影响纳米乳的理化特性。目前获FDA批准上市的两个纳米乳均为非注射用制剂,分别为Neoral(环孢素软胶囊,内容物为黄色至淡黄棕色的澄清液体)和Restasis(治疗干眼症的0.05%环孢霉素眼用乳剂)。仅一种丙泊酚注射用纳米乳(Microfol)处于临床研究中,该处方中所使用的乳化剂是辛酸钠和泊洛沙姆188。丙泊酚长链甘油三酯(LCT)脂肪乳注射剂Diprivan于1996年6月获美国FDA批准上市,临床应用时易引发高甘油三酯血症和胰腺炎等不良反应,长期输注还可导致丙泊酚输注综合征。随着中/长链脂肪乳的问世,开发了丙泊酚中长链脂肪乳注射液Propofol-Lipuro,能更快地提供能量,并具有良好的肝脏耐受性、更快的甘油三酯清除率和减轻LCT脂肪乳带来的注射疼痛等优点。2007年Daewon制药公司在韩国上市了丙泊酚纳米乳注射液Aquafol,主要的乳化剂为聚乙二醇-15-羟基硬脂酸酯(Solutol HS15)、助乳化剂为四氢呋喃、聚乙二醇醛和泊洛沙姆188。Aquafol利用常温下为液态的丙泊酚自身为油相,从而避免了脂质的使用,临床研究表明该纳米乳会产生显著的注射痛,此注射疼痛由较多的游离药物引起而非辅料所致。

图2丙泊酚脂肪乳3、脂质体注射剂脂质体(liposomes)是由磷脂和其他两亲性物质分散于水中形成的球形封闭囊泡。脂质体是通过混合特定比例的两亲性物质(如磷脂和胆固醇)形成的,当它们在水溶液中水合时,会排列成一层或多层同心的脂质双分子膜包封而成的超微型球状载体,可用于药物包载。脂质体的概念在1965年由英国Bangham等提出,1974年Rahman等首先将脂质体作为药物的载体应用。第一款脂质体注射剂是由美国NeXstar公司(已被Gilead公司并购)开发的两性霉素B脂质体Ambisome,能有效降低两性霉索B引起的急性肾毒性。Ambisome于1990年在欧洲获批上市,1997年在美国上市,用于念珠菌、曲霉菌、隐球菌等造成的深部真菌感染以及内脏利什曼病。第一款抗肿瘤药物脂质体是由美国Sequus制药公司开发的阿霉素脂质体Doxil,于1995年获FDA批准上市用于治疗进展期及铂类化疗药化疗后复发的卵巢癌患者。Doxil的组成成分中含有两亲性磷脂-聚合物共轭物聚乙二醇-硬脂酰磷脂酰乙醇胺(DSPE-PEG2000),亲水端的存在使脂质体免于被单核吞噬系统(Mononuclear Phagocytic System,MPS)快速清除而延长血液循环时间,长循环特性有利于增加脂质体在病变部位的相对蓄积量。随着新型载体材料和表面修饰技术的开发和应用,对脂质体的处方和工艺进行改进,相继开发了环境响应型、主动靶向型、长效缓释型脂质体,例如热敏脂质体、pH敏感脂质体、磁性脂质体、导向肽偶联脂质体、多肽阳离子脂质体、免疫脂质体、多囊脂质体等。目前已有多种类型的脂质体获批上市或进入临床研究阶段,相信随着技术的积累,更多优异的脂质体将会被相继开发。
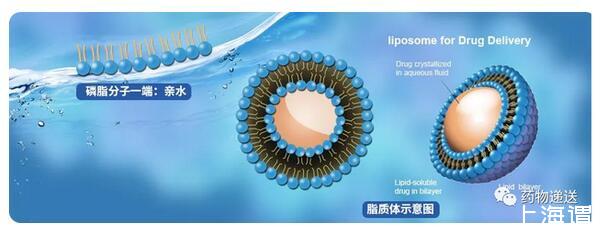
图3脂质体示意图
表3已上市的部分脂质体
脂质体具有良好的组织相容性、生物可降解性、安全性、靶向性、缓释性、制备条件温和等特点。但脂质体也存在很多缺点严重制约脂质体产品的开发和应用,例如药物包封率低、稳定性差和易发生药物泄漏、生产工艺复杂、技术要求高、质量控制难以及需要高端辅料和高精密设备等。新技术、新材料以及新载体的成功应用将极大促进脂质体注射给药系统的发展,与其他生物技术如基因工程、蛋白质工程等的结合将使药物治疗更加个性化和人性化,相信这些会进一步扩展脂质体作为药物递送载体的应用范围。










