合作客户/
拜耳公司 |
同济大学 |
联合大学 |
美国保洁 |
美国强生 |
瑞士罗氏 |
相关新闻Info
推荐新闻Info
-
> 五种表面活性剂对粉煤灰基多孔地聚物孔结构与力学性能的调控机制(二)
> 五种表面活性剂对粉煤灰基多孔地聚物孔结构与力学性能的调控机制(一)
> 粉煤灰基多孔地聚物:五种表面活性剂降低碱液表面张力与稳定泡沫的效能对比
> 表面活性剂对粉煤灰基多孔地聚物孔结构及性能的调控机制研究
> 人工模拟瘤胃体外发酵技术:纤维发酵中比表面积与表面张力的调控作用(二)
> 人工模拟瘤胃体外发酵技术:纤维发酵中比表面积与表面张力的调控作用(一)
> 翅果油饮品加工工艺的创新与深度解析界面张力仪在其中的应用
> 基于界面张力最小化优化PS微球制备工艺:SDS与Na₂SO₄浓度的选择
> 表面张力降低视角下离子液体促进气体水合物生成的机理探究
> 低用量、高效率:离子液体促进剂实现水合物生成体系表面张力最大降低53.06%
酯功能化的双子表面活性剂与血红蛋白的结合——结果和讨论
来源:上海谓载 浏览 2574 次 发布时间:2021-11-15
三、结果和讨论
3.1. 表面张力测量
表面张力测量用于研究 关于 16-E2-16/Hb 相互作用的定性信息 空气/水界面。 图 1 显示了 16-E2-16 分布的表面张力与对数浓度在不存在和 在不同温度下存在 Hb (5 μM)。 断点 表面张力与表面活性剂浓度对数的关系 不同温度下纯表面活性剂的文件对应 到相应温度下表面活性剂的 cmc。 这 16-E2-16/Hb体系的表面张力曲线呈现两个断裂 点,第一个断点对应临界聚合 浓度(cac)代表表面活性剂的开始 蛋白质结合而作为第二个断点对应于 在 Hb 存在下 16-E2-16 的 cmc。 16-E2-16 的 cmc 在不同温度下不存在和存在 Hb 的情况下 列在表 1 中。从这些值可以看出,16-E2-16 的 cmc 随着 Hb 的存在和温度升高而增加。 在 Hb 存在下 cmc 的增加证实了 16-E2-16/Hb 复合物的形成,在此期间一些单体 与 Hb 结合,因此无法形成胶束 进而导致胶束化延迟 [54]。 表1还 表明 cmc 值随温度升高而增加 这意味着疏水力的参与,它们是 温度依赖,在 cmc 的蛋白质表面活性剂相互作用中。 这可以归因于 16-E2-的溶解度增加 16 单体随温度变化而抑制胶束化。 此外,较高的温度有利于热运动,这会导致 更多的分子与 Hb 结合。 但是,cac 保持不变 在所有温度下。 因此,我们可以认为 16-E2-16 与 Hb 结合 通过 cac 附近的静电相互作用,因为静电 相互作用不受温度影响。 此后,作为 表面活性剂浓度增加,蛋白质通过疏水力与表面活性剂相互作用。 下表面张力值 Hb-16-E2-16系统比对应的16-E2-16系统是 由于 Hb 的高表面活性。
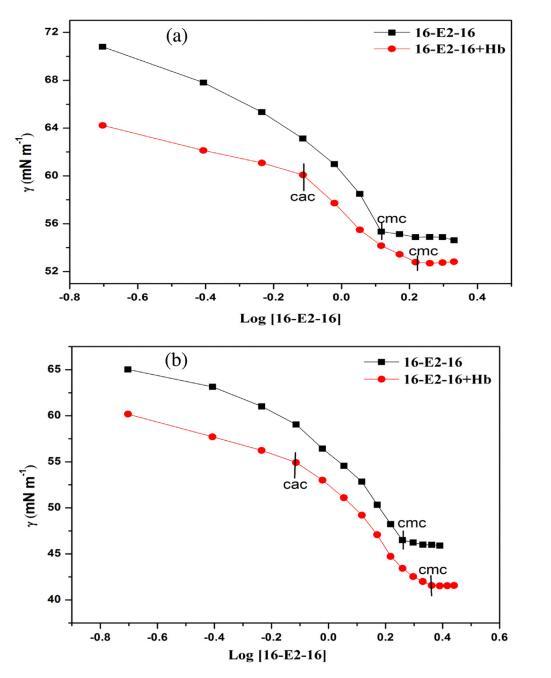
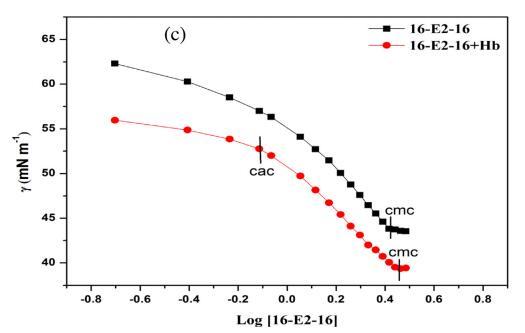
图 1. 16-E2-16/Hb 在不同温度下的表面张力。 (a) 298.15K (b) 308.15K (c) 318.15K。 [Hb] = 5 μM。
3.1.1. 界面参数
最大表面过量 (∫max) 表示为每单位面积界面处的表面活性剂分子浓度。 表面张力数据用于计算表面过量 应用吉布斯吸附等温线的浓度 (∫max) 方程:

其中 γ 是表面活性剂浓度 C 下的平衡表面张力 (mNm−1),n 是每分子的粒子数 表面活性剂。 由于表面活性剂的解离导致三种物质的形成,公式 1111 表示在低于 cmc 的恒定温度下 γ 与 log[16-E2-16] 之间的曲线斜率。 ∫max 值允许计算 每个分子 Amin 的最小表面积(以 nm2 为单位) 方程:

表格1 不同温度下 Hb 不存在和存在时 16-E2-16 的 cmc、∫max 和 Amin
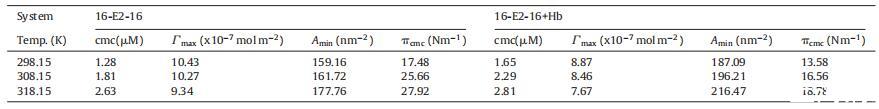
其中 NA 是阿伏伽德罗数。 为 ∫max 获得的数据 和 Amin 列于表 1。发现 ∫max 值为 16- E2-16 随温度升高而降低,表明 系统涉及静电和疏水相互作用[55]。 Amin 值随温度升高而增加 正如分子运动增加所预期的那样 [56]。 ˘cmc ,其定义为表面活性剂降低表面张力的有效性,测量为 cmc 处的表面压力 [57],和 从关系计算:

其中γ o 和γ cmc 是指溶剂体系的表面张力 (水/水 + Hb) 和 cmc 值下溶液的表面张力。
3.1.2. 热力学参数
离子表面活性剂在水溶液中胶束化的热力学参数可以借助 以下方程使用质量作用模型胶束化 [58]

其中αG0m、αH0m和αS0m是自由能、焓的变化 和胶束化熵,Xcmc 是 cmc 处的摩尔分数。 这 从方程 (6-8) 获得的值显示在表 2 中。
表 2 胶束化的自由能 (αG0m)、熵 (αS0m) 和焓 (αH0m) 的变化以及自由能 (αG0) 的变化 ad) 不存在和存在时 16-E2-16 的吸附 不同温度下的 Hb。
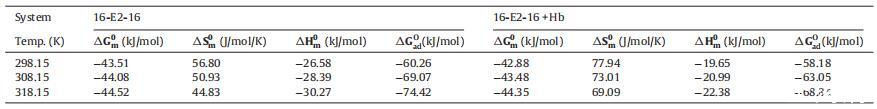
这 αG0m 在所有温度下的负值表明容易 在所研究的条件下形成胶束。 此外, αG0m 的负值随温度升高而增大 这表明16-E2-16分子在高温下脱水是胶束形成的主要因素。 这 胶束化 αH0m 的负值证实了放热 过程的性质。 获得的 αS0m 值都是正的,表明系统在转换后增加了随机性 离子表面活性剂分子变成胶束。 换句话说,我们可以 说对表面活性剂的运动有较小的阻碍 分子存在于胶束中时。
标准吸附自由能,αG0 这个系统的广告是 使用关系计算:

αG0 的值 由此获得的 ad 列于表 2 中。 吸附热力学参数αG0 广告价值全是 负且比 αG0m 更负,表明界面处的吸附与自由能的降低有关 系统的。 这可能是由于空间因子对 对胶束化的抑制作用大于对吸附作用的影响。
3.2. 紫外-可见研究
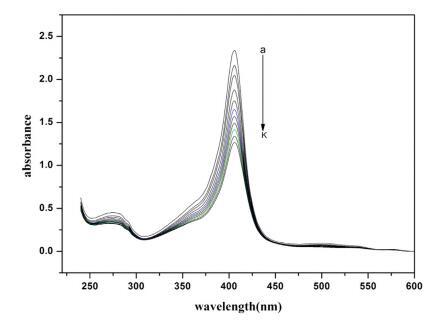
Hb 在其吸收光谱中显示三个不同的峰。 这些 是; Trp 和 Tyr 残基的苯基(273 nm), -乐队 (360 nm) 和卟啉-索雷带 (404 nm,强烈允许 - * 电子跃迁)[59,60]。 这个乐队起源于 血红素基团,嵌入由 蛋白质的骨架通过适当的折叠[61,62]。 变化 soret 吸收带的位置和强度 提供有关蛋白质在缀合过程中可能发生解折叠和变性的信息 [59,60,62,63]。 图 2 显示了 不存在和存在各种浓度的 Hb 的吸光度 16-E2-16。 添加 16-E2-16 显示出显着的 Soret 带强度的光谱变化,但峰值位置保持不变。 16-E2-16 降低强度 soret 带暗示 16-E2-16 可以访问血红素组 并直接参与扰乱结构和暴露 水介质中的血红素基团 [61]。 换句话说我们 可以说,由于蛋白质的血红素基团与 16-E2-16 的某种相互作用,Hb 经历了扰动。 血红蛋白是 由于工作 pH 值 (7.4) 较大,因此带轻微负电荷 比 Hb 的 pI (6.86) 和在这种情况下阳离子的相互作用 表面活性剂与蛋白质同时具有静电和疏水性 [64] 然而,这与表面张力结果非常吻合,van 德瓦尔斯力不容忽视。
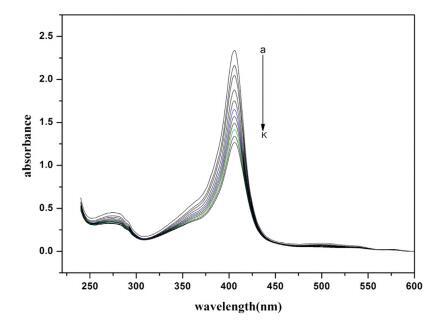
图 2. 不存在和存在 16-E2-16 时 Hb (5 μM) 的紫外-可见光谱。 这 16-E2-16 (am) 的浓度为 0, 0.39, 0.76, 1.13, 1.48, 1.81, 2.14, 2.45, 2.75, 3.05 和 3.33 μM。
3.3. 荧光光谱研究
Hb 的荧光主要是由于色氨酸和酪氨酸残基的存在。 图 3 显示了荧光光谱 Hb 不存在和存在 16-E2-16。 每个 α 和 ˇ 链中有 3 个色氨酸(α214Trp、β215Trp、β217Trp)。 根据 Rodgers 的说法,[65] Hb 的内部荧光主要是 来源于 β237Trp。 由于 Trp 和血红素都位于 在 Hb 的疏水腔中,有效的能量转移来自 Trp 到血红素显着淬灭蛋白质荧光 [66] 因此,水中 Hb 的荧光强度非常低。 当用不同量滴定固定量的 Hb 时 在 16-E2-16 中,Hb 荧光强度的增加是 观察到(图 3)表明表面活性剂分子渗透 Hb 的疏水腔并暴露血红素,从而 用血红素抑制 Trp 猝灭,从而抑制荧光 Hb 强度明显增加。 最初,荧光 强度迅速增加,但当 16-E2-16 的浓度 超过它的cmc,荧光强度缓慢增加 此后。 对这一观察结果的合理解释是 疏水腔中疏水血红素的溶解 表面活性剂胶束增加血红素之间的距离 和 trp 并以这种方式抑制了 Trp 之间的能量转移 和血红素。
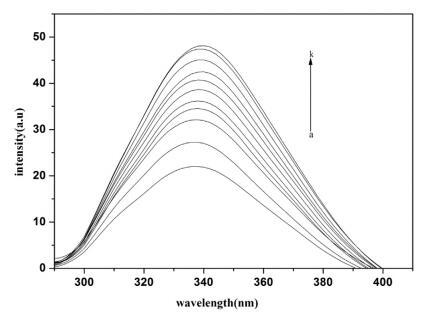
图 3. 不存在和存在 16-E2-16 时 Hb (5 μM) 的荧光光谱。 这 16-E2-16 (ak) 的浓度为 0, 0.39, 0.76, 1.13, 1.48, 1.81, 2.14, 2.45, 2.75, 3.05 和 3.33 μM。
图 4 为 Hb 的同步荧光光谱 16-E2-16 在水体系中,μ = 20 nm(图 4a)和 γ? = 80 nm(图 4b)。 当 μ= 20 nm 时,特征信息 关于Tyr,当γμ= 80 nm 时,获得关于Trp 的特征信息[67]。 从图中可以看出 Tyr 和 Trp 的荧光强度增加,荧光发射波长几乎保持不变 添加 16-E2-16。 从图 4(a 和 b)可以看出,Trp 的荧光强度增加大于 Tyr。 因此,Trp 荧光可以代表 Hb 荧光 16-E2-16/H2O 系统。
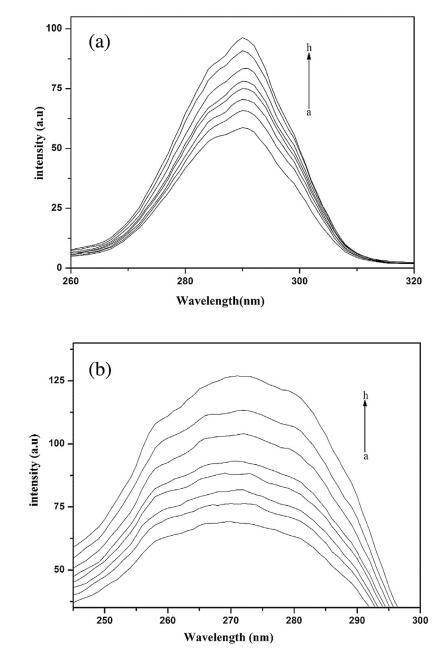
图 4. Hb (5 μM) 的同步荧光光谱。 (a) α∫= 20 nm (b) ? = 80 纳米。 16-E2-16(ah)的浓度分别为0、0.39、0.76、1.13、1.48、1.81、 2.14 和 2.45,μM。
3.4. 圆二色性
进行CD以进一步确认构象变化 由 16-E2-16 引起的 Hb,从而允许进一步评估 Hb 和 16-E2-16 之间的相互作用。 图 5 显示了 不存在和存在 16-E2-16 时 Hb 的 CD 光谱。 光盘 Hb 的光谱在 208 nm 和 222 nm 处显示两个负最小值, 蛋白质α-螺旋结构的特征。 16-E2-16 光学不活动不显示任何信号。 在场 在 16-E2-16 中,Hb 的负椭圆度降低,表明 可能形成 Hb/16-E2-16 复合物 [68]。 α-螺旋 计算了 Hb 及其与 16-E2-16 (2 μM) 复合物的百分比,发现分别为 53% 和 47%。 进一步降低 在更高浓度的 16-E2-16 (2.5 μM) 存在下达到 44% 表明 Hb 的 α-螺旋含量明显降低。 因此, CD 结果表明存在 16-E2-16 变化 Hb 的二级结构与我们的 计算结果。
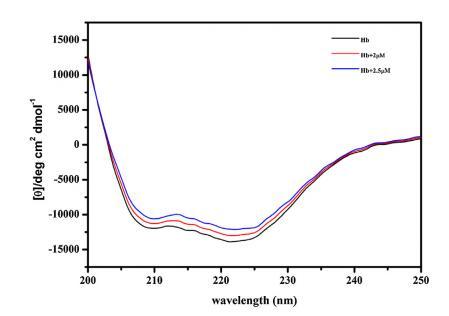
图 5. 不存在和存在 16-E2-16 时 Hb (5 μM) 的 CD 光谱。
3.5. 分子对接
Hb 中的 α 和 β 链具有相似的结构折叠, 由七个连续的α-螺旋和两条链组成 包含由螺旋 4 和 5 包围的间隙结合袋,而空腔的底部由 C 端部分形成 螺旋 6 和螺旋 7 的 N 端片段 [69]。 16-E2-16为主 Hb 与中央空腔、α1 和 β2 链结合(图 6A)。 这 该结合位点上的氨基酸残基包括 Thr39, α1 中的 Tyr42、Phe43、Pro44、His45、His58、His87、Leu91、Val93、Asn97 链和 Leu31、Arg40、Phe41、Phe42、His63、Val67、Ala70、Phe71、 His92, Leu96, His 97, Val98, Asn102, Phe103, Leu106, Leu141 in β2 链图 6B。 有超过 20 个氨基酸残基位于 16-E2-16 的站点,这意味着它们之间的强相互作用 16-E2-16 和 Hb [70]。 疏水性和静电力作用 在 16-E2-16 与 Hb 的结合中起重要作用,这个结果是 与我们的实验结果一致。 然而,范德瓦尔斯 力量不容忽视。 已观察到一个氢键 在 16-E2-16/Hb 相互作用中的 16-E2-O 原子 具有 β2 链 ARG40 的 16 个分子(图 6C)。 的形成 氢键稳定 16-E2-16/Hb 复合物。 的类型 相互作用和参与相互作用的氨基酸残基 以表格形式显示(表 3)。
表3 结合能、结合常数和活性位点残基及其与配体的相互作用类型。
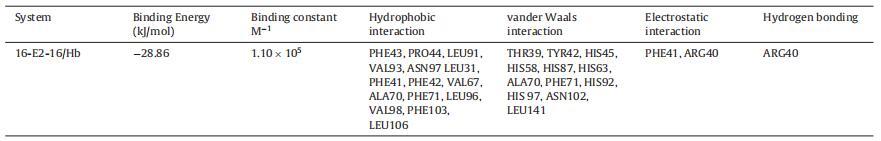
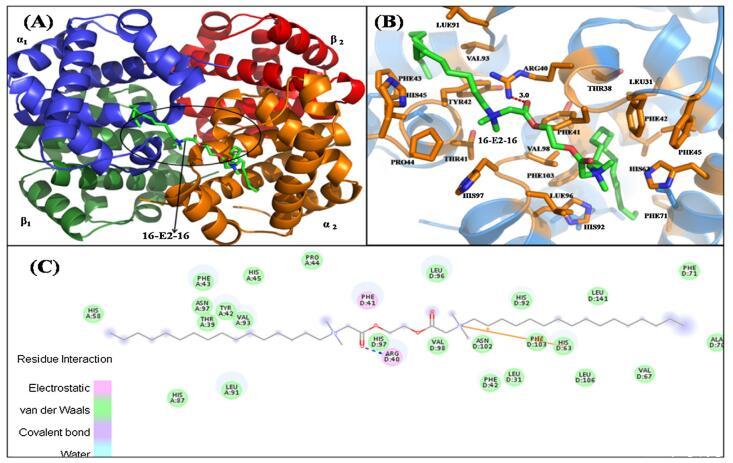
图 6. 具有 16-E2-16 的 Hb 结构示意图。 (A) Hb-16-E2-16 的结构。 Hb 的亚单位用不同的颜色表示。 配体 16-E2-16 是 以棍子为代表。 (B) 距停靠的 16-E2-16(绿色)5Å 范围内 Hb 的周围氨基酸残基(橙色)。 (C) Hb/16-E2-16 相互作用的二维表示。 (为了 对图例中颜色参考的解释,读者可参考本文的网络版本。)
3.6. 分子动力学模拟
进一步研究16-E2-16的结构稳定性影响 结合Hb,采用分子动力学模拟。 我们分析了两者的动态结构特性,例如均方根偏差 (RMSD) 和回转半径 (Rg)。 未绑定和 16-E2-16 有界 Hb 使用从获得的轨迹 MD模拟。
为了探索 Hb 的稳定性和动力学特性 绑定后,未绑定和16-E2-16有界的MD模拟 Hb 是针对 20000 ps 的模拟时间尺度进行的。 图 7(A) 显示未结合和 16-E2-16 的 RMSD 值 有界 Hb 复合物从 0 ps 突然增加到 6000 ps 并且 此后两个系统都达到平衡相并获得 在整个仿真过程中,RMSD 值稳定,波动小。 未结合和 16-E2-16 有界 Hb 的 RMSD 值 分别为 0.38 ± 0.02 和 0.34 ± 0.01 nm,在 最后 10000 ps 轨迹。 因此,很明显 16-E2-的 RMSD 值 16 有界 Hb 小于未结合 Hb。 这一结果表明 16-结合后的结构变化和复合物形成 E2-16 与 Hb 显示出与我们的 UV-vis 的良好一致性 结果 [71]。
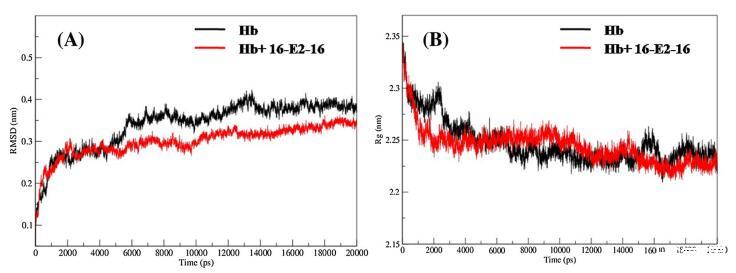
图 7. (A) RMSD 和 (B) Rg 随未结合和 16-E2-16 有界 Hb 的模拟时间的变化。
Rg 值给出了整体结构的精细测量 Hb 的维度。 未结合和 16-E2-16 有界 Hb 在模拟 20000 ps 时间尺度上计算的 Rg 值 如图7(B)所示。 该图清楚地表明,最初未结合的和 16-E2-16 有界的 Hb 具有相同的 Rg 值 (2.34 nm) 并在 4000 ps 左右达到平衡,此后为 Rg 值在整个模拟期间保持稳定,波动很小。 该 Rg 值与报告的 Hb 的 Rg 值相似 (2.37 ± 0.05 nm) 通过中子散射技术测量 水溶液[72-75],因此表明模拟结果的准确性。 达到平衡后,未结合的 Rg 值和 发现 16-E2-16 有界 Hb 为 2.22 ± 0.02 和 2.21 ± 0.02 分别在整个模拟过程中波动很小。 从 6000 到 12000 ps,16-E2-16 结合 Hb 的 Rg 值有 略有增加,而从 14000 到 20000 ps,Rg 值减少 关于未结合的 Hb。 Rg 值的这种变化表明 16- E2-16 在 Hb 中引起了一点构象变化 [68],这 与实验结果相似,与CD吻合良好 结果。










