合作客户/
拜耳公司 |
同济大学 |
联合大学 |
美国保洁 |
美国强生 |
瑞士罗氏 |
相关新闻Info
推荐新闻Info
-
> 五种表面活性剂对粉煤灰基多孔地聚物孔结构与力学性能的调控机制(二)
> 五种表面活性剂对粉煤灰基多孔地聚物孔结构与力学性能的调控机制(一)
> 粉煤灰基多孔地聚物:五种表面活性剂降低碱液表面张力与稳定泡沫的效能对比
> 表面活性剂对粉煤灰基多孔地聚物孔结构及性能的调控机制研究
> 人工模拟瘤胃体外发酵技术:纤维发酵中比表面积与表面张力的调控作用(二)
> 人工模拟瘤胃体外发酵技术:纤维发酵中比表面积与表面张力的调控作用(一)
> 翅果油饮品加工工艺的创新与深度解析界面张力仪在其中的应用
> 基于界面张力最小化优化PS微球制备工艺:SDS与Na₂SO₄浓度的选择
> 表面张力降低视角下离子液体促进气体水合物生成的机理探究
> 低用量、高效率:离子液体促进剂实现水合物生成体系表面张力最大降低53.06%
酯功能化的双子表面活性剂与血红蛋白的结合——摘要、简介
来源:上海谓载 浏览 2113 次 发布时间:2021-11-15
摘要
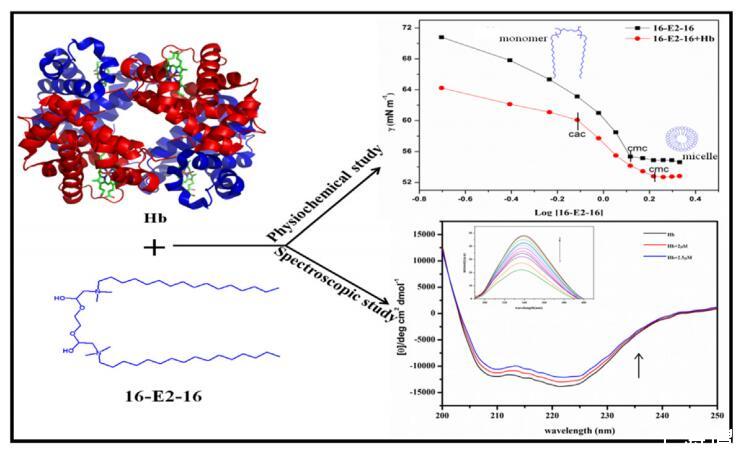
荧光、紫外-可见光、圆二色性 (CD) 光谱和表面张力技术 用于研究血红蛋白 (Hb) 和双子表面活性剂 bis (N, N-二甲基-N-十六烷基乙酸铵)二氯化物(16-E2-16)。 分子对接与模拟 还研究了与 16-E2-16 相互作用时 Hb 构象的变化。 这 UV-vis 研究证明了 soret/血红素带的扰动,并在 16-E2-16 存在的情况下在血红素组内产生构象异质性。 数据显示荧光增加 添加 16-E2-16 后 Hb 的强度。 16-E2-16的cmc值后荧光 强度缓慢增加。 Trp 荧光比 Tyr 的影响更大。 临界胶束 测定了不同温度下 Hb 不存在和存在时 16-E2-16 的浓度 使用表面张力图。 cmc 随温度升高以及存在而增加 的 Hb。 此外,还研究了胶束化的热力学参数。 对接研究 表明 16-E2-16 结合 Hb 的 α1 和 β2 链,主要作用力是疏水的 和静电。 模拟和 CD 研究证实了结合后 Hb 的构象变化 与 16-E2-16。
一、简介
在所有血红素蛋白中,血红蛋白是被广泛研究的蛋白质。 它由两条α链和两条β链组成, 每条链形成一个疏水空间,保护血红素 来自水的单体 [1]。 它的分子量为 64.5 KDa 和 含有大量可电离的氨基酸,这使得它 极易溶于水。 发现血红蛋白结合许多不同类型的两亲分子,这些分子起重要作用 在确定生理功能 [2-7]。 因为,许多不同的两亲组件,如胶束、囊泡、管和层状 液晶等常用于模拟一些生物系统,因此它们与 Hb 的相互作用可以提供有趣的 有关 Hb 的热力学、结构、生物医学和生物物理信息 [8-10]。 与他人互动的研究 分子,如细菌内毒素 [11,12]、羟基脲 [13] 和海藻糖 [14],表明某些生物分子可以 将氧合血红蛋白 (oxyHb) 转化为高铁血红蛋白 (metHb) 和 半色素,而其他一些可能减缓或逆转 Hb 的自氧化过程 [12,14]。
蛋白质与表面活性剂的相互作用很常见 在化学、生物学和医学领域[15-17]。 超过 在过去的几十年里,蛋白质-表面活性剂的相互作用 由于其在工业、生物学和制药方面的重要性而成为广泛研究的主题 [18,19]。 有关的信息 蛋白质-表面活性剂复合物的结构已经推导出来 来自流变学 [20]、光谱学 [20,21]、电泳 [22]、 结合 [23,24] 和散射研究 [25,26]。 最近,该研究 表面活性剂与蛋白质相互作用的研究 表面活性剂-蛋白质复合物结构及其变化 蛋白质结构。 疏水相互作用、静电相互作用、范德华力和氢键起着重要作用 在配体-蛋白质结合中的作用 [27]。 疏水性促进水 去除并支持蛋白质-配体相互作用,但它也调节介电效应。 如果蛋白质和配体带有一些电荷 那么静电相互作用确实在蛋白质配体结合中起重要作用。 范德华相互作用形成于 永久偶极子或相应的感应偶极子相互作用。 这 这些相互作用的影响在可极化基团中最高 蛋白质,它包括存在于 疏水性氨基酸,如亮氨酸和缬氨酸。 这种互动 与距离有关,并随着距离增加 5Å 而减少。 在蛋白质-配体相互作用中,氢键也起着重要作用。 Babine 和 Bender 报道了氢键 对蛋白质-配体复合物的稳定性有很大贡献[28]。
一般而言,CMC以下的离子表面活性剂(阳离子和阴离子) 与蛋白质的带相反电荷的残基结合。 阳离子表面活性剂通常与谷氨酸 (glu) 和天冬氨酸 (asp) 结合 蛋白质的残基与它们产生静电和疏水相互作用。 随着表面活性剂的浓度 增加,表面活性剂分子开始形成簇 使蛋白质的结合位点饱和,从而导致蛋白质解折叠。 这些簇经常与蛋白质分子相互作用 稳定他们。 蛋白质通过表面活性剂展开 取决于表面活性剂浓度之间的比率 和蛋白质,这个比例决定了多少表面活性剂可用 每个蛋白质分子。 因此,展开随着增加 表面活性剂分子的浓度,在这个阶段表面活性剂 作为典型的变性剂 [29]。
最近,已经设计和开发了新的表面活性剂。 这些表面活性剂由两条疏水链和 两个极性头部基团通过间隔基团共价连接 [30–33]。 这种新型表面活性剂被称为双子表面活性剂。 它们表现出与传统表面活性剂不同的特性, 例如较低的临界胶束浓度 (cmc)、对间隔结构的强烈依赖、特殊的聚集体形态和强疏水微域 [34,35]。 因此,相比 与常规表面活性剂相比,双子表面活性剂表现出不同的 与蛋白质的行为。 此外,双子表面活性剂可以减少洗涤剂对环境的影响, 因为执行相同的操作所需的量要少得多 功能。 此外,它们不寻常的效率和化学多功能性将 对设计新型浓缩洗涤剂有很大的方便。 我们小组最近致力于研究双子表面活性剂与不同蛋白质的相互作用 [36-38]。
继续,在此,我们研究了基于酯的相互作用 阳离子双子表面活性剂 (16-E2-16) 与 Hb 使用表面张力、UV-vis 和荧光。 16-E2-16 中含有一个酯键 并且发现在本质上是可切割的,因为较高的 极性键有助于提高水溶性,使其 容易降解 [39,40] 间隔基中的酯键使 与其他阳离子表面活性剂相比,gemini 更易裂解、可生物降解且水生毒性更低 [41,42]。 还有酯 双子座中的键促进与蛋白质的氢键结合 [38]。
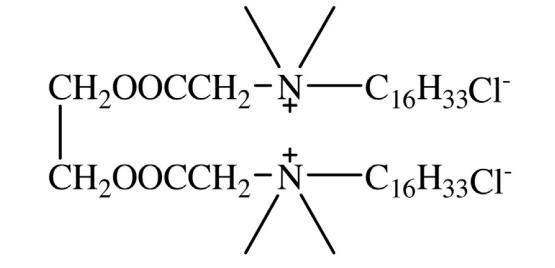
方案 1. 16-E2-16 的结构。