合作客户/
拜耳公司 |
同济大学 |
联合大学 |
美国保洁 |
美国强生 |
瑞士罗氏 |
相关新闻Info
推荐新闻Info
-
> 界面扩张黏弹性与驱油机理研究进展
> 蛋白质聚集与表面张力:界面行为、聚集机制及测量技术前沿
> 动态光散射法(DLS)在临界胶束浓度(CMC)测定中的原理、应用与最新进展
> 溶液吸附作用与表面张力测定:从理论到实践的完整指南
> 面向水基农药制剂的新型表面活性剂TPGS-X-M动静态表面张力及性能研究
> 表面活性剂TPGS-X-M的合成及表面张力测试
> 用于水基性农药制剂的新型绿色表面活性剂合成路径及表面张力测定
> 超微量天平在药物研发中的应用:精确称量活性成分与标准品
> 超微量天平工作原理,如何为药物研发实验室选择超微量天平?
> 醇醚硫酸盐泡排剂的耐温耐盐性能及分子机理研究
葡萄酒的表面张力与酒本身的成分之间的相关性论文——结果与讨论
来源:Unisense 浏览 2450 次 发布时间:2021-09-15
结果与讨论
3.1. 模型解测量
为了突出葡萄酒主要成分对表面张力的影响,制备了乙醇、蛋白质和单宁标准溶液,并在三种不同的基质中测定了它们的表面张力:水、水/乙醇混合物(12%,v/v 乙醇)和模型葡萄酒溶液(12%,v/v 乙醇,2 g/L 酒石酸,pH 3.5)。 研究的浓度在通常在葡萄酒中发现的范围内。 选择 BSA 作为参考蛋白质,代表表面活性蛋白质。 众所周知,BSA 具有与广泛使用的表面活性剂十二烷基硫酸钠 (SDS) 相当的优异发泡性能(Razafindralambo 等,1996)。 结果如表 1 所示。使用市售的酿酒单宁(从葡萄皮和种子中提取的单宁的天然混合物),因为它们被认为是葡萄酒中天然存在的单宁的代表。 结果如图1所示。
表 1 乙醇和 BSA 标准溶液在水、水/乙醇混合物(12%,v/v 乙醇)和模型葡萄酒溶液(12%,v/v 乙醇,2 g/L 酒石酸,pH 3.5)中的表面张力值25岁。
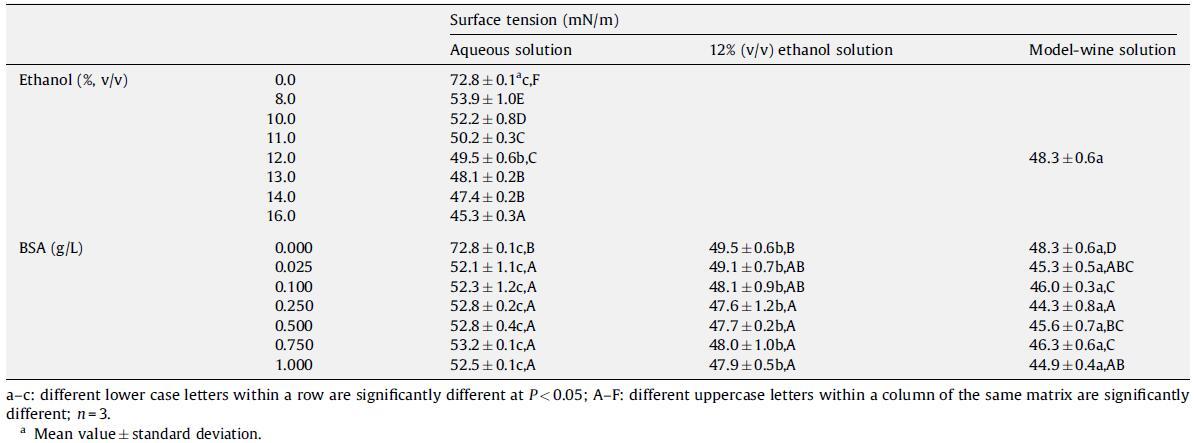
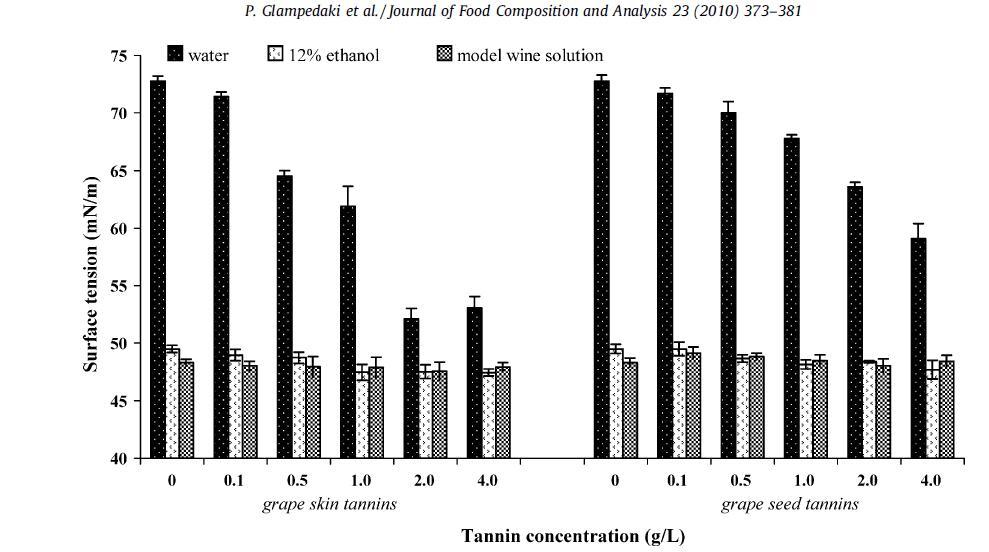
图 1. 酿酒葡萄皮和种子单宁在水、水/乙醇混合物(12%,v/v 乙醇)和模型葡萄酒溶液(12%,v/v 乙醇,2)中的表面张力值(25 度) g/L 酒石酸,pH 3.5)。 结果表明平均值 ? 标准偏差(n = 3)。
发现去离子水的表面张力在 25 ℃ 时等于 72.8 ± 0.1 mN/m。 普遍接受的普通水表面张力值等于 71.98 +- 0.36 mN/m at 25°(普通水物质表面张力的 IAWPS 释放,1994),而在 25° 报道的值从 71.82 mN/m( Douglas, 1950) 到 73 mN/m (Smith 和 Sorg, 1941)。 观察到的差异可能是由于分析中使用的水类型(普通水、蒸馏水和去离子水)、系统中存在的痕量杂质或测量方法的不确定性(Gaonkar 和 Neuman,1987 年)。 乙醇的加入显着降低了水的表面张力——这种有机化合物的影响之前已经被研究过(Janczuk 等人,1985 年;Va´zquez 等人,1995 年)。 对于 12% (v/v) 的平均乙醇含量,标准溶液的表面张力比去离子水低 20 mN/m 以上(分别为 49.5 ± 0.6 和 72.8 ± 0.1 mN/m)。 另一方面,10% (v/v) 溶液(在 25 度,等于 52.2 ± 0.8 mN/m)的表面张力比去离子水低 20.6 mN/m(表 1); 这与 Jin 等人获得的值相当。 (2009)(5% 和 10% (v/v) 乙醇-水溶液分别为 59.7 和 53.4 mN/m,温度为 20 +- 1 冷却)。 在模型葡萄酒溶液中,测得的表面张力值略低 (48.3 mN/m),这可能是由于添加了酒石酸。 酒石酸水溶液(2g/L)的表面张力经测量为69mN/m。
关于 BSA 溶液,观察到表面张力值的显着变化。 随着 BSA 含量的增加,不仅在同一基质内发现差异,而且在三种不同基质之间也存在差异(表 1)。 正如预期的那样,所使用的白蛋白表现出很强的表面活性,并导致溶液表面张力显着降低,测得的最低值 (44.3 mN/m) 是含 0.250 g BSA/L 的模型酒溶液的值。
在水醇 BSA 溶液中,测得的值从 49.1 到 47.6 mN/m(平均值为 48.1 mN/m),表明蛋白质对乙醇已经引起的作用的贡献。 乙醇溶液的极性低于水,因此,蛋白质可能会改变其折叠方式,以增加其表面疏水性和柔韧性,在基质中存在醇的情况下变得更具表面活性。 这可以证明观察到的 BSA 水醇标准溶液的表面张力值降低是合理的。 所有溶液中最低的表面张力值是在 BSA 模型葡萄酒溶液中测得的(46.3–44.3 mN/m,而相应的对照溶液中为 48.3 mN/m)(表 1)。 这可能归因于模型溶液的标准化 pH 值(等于 3.5),这显然影响了电荷,因此影响了白蛋白在此特定基质中的构型和溶解度。 根据文献数据,在低于白蛋白等电点 (pI = 4.7) 的 pH 值下,螺旋分子构型发生显着变化,分子内键断裂,分子展开,使蛋白质更具疏水性,因此具有更高的表面活性 (Foster , 1960)。
在单宁标准水溶液的情况下,从图 1 中可以明显看出,与葡萄籽单宁相比,葡萄皮单宁引起的表面张力降低更大。 观察到葡萄皮单宁比葡萄籽单宁更具表面活性,部分原因可能是前者具有更高的聚合度,因此比后者更疏水(Poncet-Legrand 等,2003;Crespy, 2006)。 在其他两个溶液系列(水醇和模型酒)中,乙醇的存在再次增加了表面张力值,而单宁的添加进一步降低了表面张力仅 1.5 mN/m(与具有表面张力的相应对照溶液相比)分别等于 49.5 和 48.3 mN/m)。 观察值与书目数据一致,给出的表面张力等于 48.4 ? 12% (v/v) 的葡萄籽单宁乙醇溶液为 0.05 mN/m(Poncet-Legrand 等,2003)。 此外,相同的参考文献提到浓度高于 1 g/L 时会形成葡萄单宁分子的胶体聚集体,这为最后三种标准溶液(1.0、2.0 和 4.0 g)获得的相似表面张力值提供了可能的解释。单宁/L)的水醇和模型酒系列。
3.2. 表面张力与葡萄酒分析参数之间的统计相关性
检测到乙醇、蛋白质和单宁对水性、水醇和模型葡萄酒标准溶液的表面张力有显着影响,以及上述基质之间的重要变化后,我们认为继续对真实葡萄酒样品进行研究很有趣。 我们的目标是评估尽可能多的其他葡萄酒化合物对表面张力的影响,获得统计相关性,最后,基于对葡萄酒表面张力的简单测量,获得基本酿酒参数值的预测模型。
表 2 在 20 个葡萄酒样品中测定的分析参数的平均值。
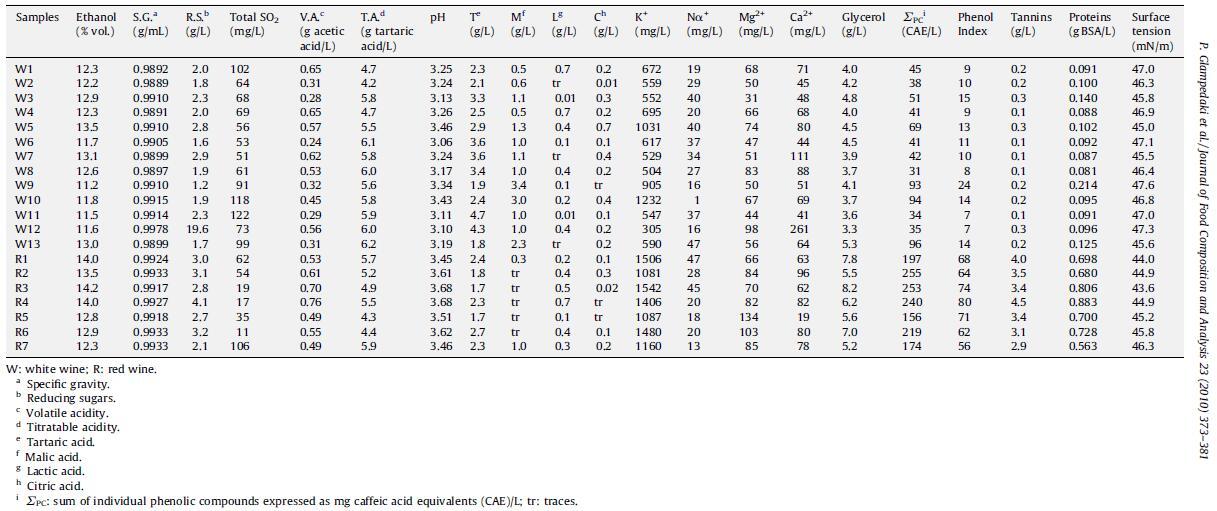
为此,对 20 种静止、白色和红色希腊单品种葡萄酒样品进行了常规酿酒学参数(乙醇含量、比重、还原糖、可滴定酸度、挥发性酸度、总 SO2 和 pH 值)和表面张力的测定。 还进行了使用 HPLC 测定有机酸(酒石酸、苹果酸、乳酸和柠檬酸)、阳离子(钾、钠、镁和钙)、甘油和酚类化合物以及使用气相色谱法测定挥发性化合物的基本仪器分析。 最后,采用光谱法进行总酚指数、单宁和蛋白质测定。 结果如表 2 和表 3 所示。关于蛋白质测定,可能影响所有样品的系统分析误差可视为不影响最终值,因为所研究的葡萄酒具有相似的乙醇含量。 此外,在葡萄酒样品中加入已知量的标准 BSA 溶液进行的分析未发现对蛋白质测定有任何干扰(数据未显示)。 上述数据与表面张力的相关性分析结果如表4所示。
葡萄酒的表面张力值在 43.6 到 47.6 mN/m 之间变化(表 2)。 平均而言,白葡萄酒的表面张力值高于红葡萄酒(平均值分别为 46.5 和 45.0 mN/m),这一结果与文献非常一致(Andre´s-Lacueva 等,1997;Pe´ ron 等人,2000 年)。 乙醇含量最低(11.2%)的样品 W9(白葡萄酒)表现出最高的表面张力值(47.6 mN/m),而酒精强度最高(14.2%)的样品 R3(红葡萄酒)表现出最低的表面张力值张力值 (43.6 mN/m),考虑到乙醇对表面张力的影响,这是预期的结果。 样品 R3 还含有非常丰富的蛋白质和单宁,如前所述,这两种成分都会降低表面张力。 该特定样品还含有高浓度 (8.2 mg/L) 的甘油。
表 3 在 20 个葡萄酒样品中测定的挥发性化合物浓度的平均值。
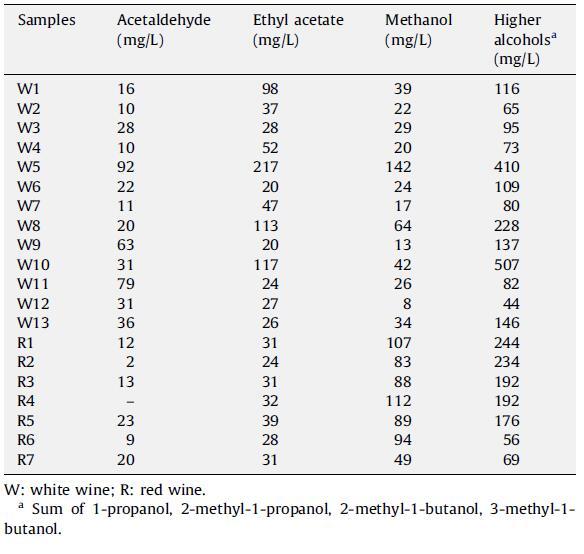
统计分析显示,在检查的 24 个分析参数中,有 12 个与表面张力显着相关(P < 0.05)(表 4)。 其中有 10 个(乙醇、蛋白质、单宁、挥发性酸度、pH、钾、钠、甲醇和总酚——280 nm 吸光度和 HPLC 测定)具有负相关系数,表明它们与表面张力成反比,较高的它们的值,样品的表面张力越低。 另外两个(苹果酸和总 SO2)具有正相关系数。 测量的最小 P 值 (P = 0.000000) 对应于乙醇,第二小 (P = 0.000476) 对应于单宁,表明这两个参数与表面张力的相关性最好。 不出所料,还原糖和比重根本没有关联,因为糖分子表现出高水溶性并且几乎没有表面活性。
表 4 在 95% 置信水平 (n=25) 下表面张力和化学变量之间的平均值、相关系数 (r) 和决定系数 (R2)。
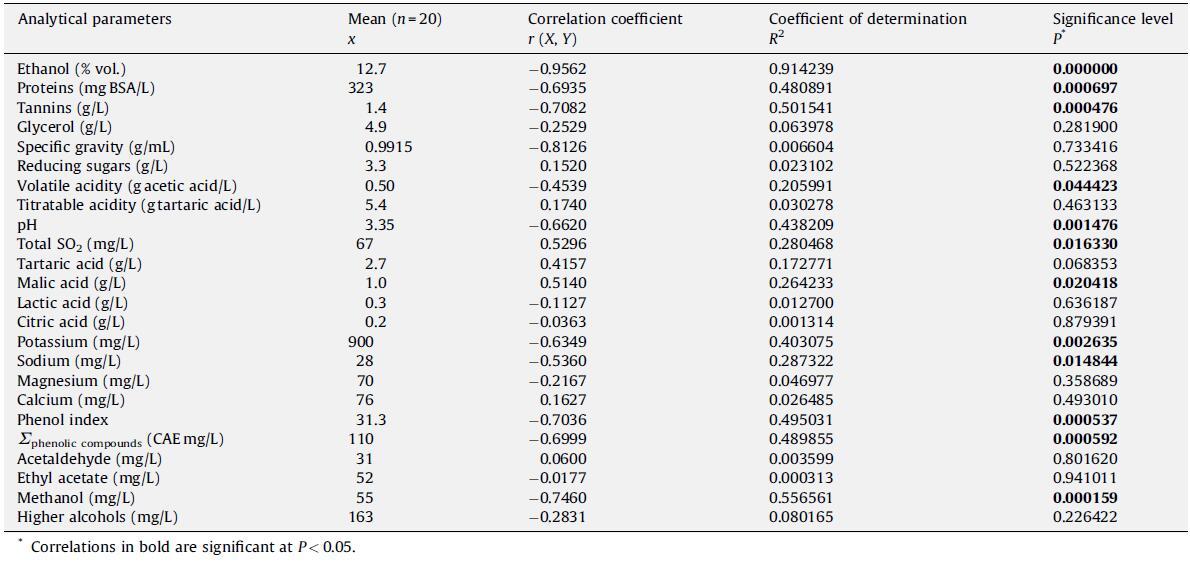
与其他研究一致,乙醇对葡萄酒的表面张力起着关键作用(Pe´ron 等人,2000 年;Liger-Belair,2005 年)。 尽管它不是典型的表面活性剂——即具有疏水链、亲水链和临界胶束浓度的分子 (Myers, 1988)——乙醇在葡萄酒中的浓度很高,实际上控制着表面张力值的基本变化。 因此,对于酒精浓度为 12% 的葡萄酒,表面张力预计约为 49.5 mN/m(表 1)。 然而,实际上这种情况很少发生。 为了解释样品与样品之间平均值的轻微增加或减少,有必要考虑其他表面活性葡萄酒化合物(如蛋白质和单宁)的存在和影响。 蛋白质,虽然在葡萄酒中发现的数量很少(几毫克/升),但具有非常重要的表面特性,可以显着降低其表面张力。 单宁由于其芳香环和非离子中心 -O-(Poncet-Legrand 等,2003)也具有表面活性剂特性,尽管它们的临界胶束浓度(胶束形成点)尚未确定。 Andre´s-Lacueva 等人。 (1997) 描述了蛋白质和单宁之间的结构相互作用,可增强起泡酒中的泡沫稳定性。 在我们的研究中进行的统计分析表明,上述参数与表面张力之间存在这种相关性(所有三个 P 值均显着低于 0.05:Pethanol = 0.000000;Pprotein = 0.000697;Ptannin = 0.000476)。
本研究中通过 HPLC 测定的单个酚类化合物的总和(花青素、儿茶素和表儿茶素)也与表面张力高度相关(P = 0.000592)。 据几位研究人员称,葡萄酒多酚会与蛋白质和多糖相互作用,从而影响其表面特性(Segarra 等,1995;Frazier 等,2003;Poncet-Legrand 等,2003;Viljanen 等,2005)。 最后,苯酚指数是指所有在其分子中具有苯环的化合物,因此在 280 nm 处具有最大吸光度,与 P = 0.000537 显示出非常好的相关性。 从这些结果可以看出,酚类化合物(简单分子以及单宁等复杂分子)会影响葡萄酒的表面张力,并且它们在葡萄酒中的浓度越高,后者的表面张力就越小。
挥发性酸度、pH、钾、钠和甲醇也与表面张力相关(表 4)。 众所周知,pH 值会影响一些最基本的葡萄酒化合物,更具体地说,影响不同形式的二氧化硫、电离形式的花青素或蛋白质构型之间的平衡。 例如,在代表葡萄酒的 pH 值约为 3.50 时,葡萄酒蛋白质——其中绝大多数表现出低等电点(4.1 < pI < 5.8)(Ferreira 等人,2002)——看起来更疏水,即更多的表面活跃(Brissonnet 和 Maujean,1993 年)。 这种效应可以部分解释与表面张力相关的 pH 值 P = 0.001476。 另一方面,pH 值本身受电解质存在的影响。 由于葡萄酒中最重要的盐是酒石酸与钾和钠阳离子的盐,它们对 pH 值的影响显然也对表面张力有影响。 这可能就是为什么相应的 P 值为 PK + = 0.002635 和 PNa + = 0.014844,远低于 0.05 的原因。 就挥发性酸度而言,我们知道同系乙酸的脂肪酸具有离子化的羧酸头,因此它们可以影响表面张力值的变化。 最后,之前的研究提到了高级醇和某些挥发性酯与葡萄酒表面张力的相关性(Andre´s-Lacueva 等,1996a;Liger-Belair,2005)。 然而,在本研究中,甲醇首次在统计上与表面张力直接相关。
其他研究人员也提出了苹果酸和表面张力之间的相关性,如值 P = 0.020418 (<0.05) 所示(Andre´s-Lacueva 等人,1996a)。 正相关系数反映在样品的分析特性上。 例如,具有最高表面张力值 (47.6 mN/m) 的 W9 样品的苹果酸浓度也最高 (3.4 g/L),如表 2 所示。这也表明在生产过程中潜在的苹果酸乳酸发酵静止葡萄酒可以降低最终产品的表面张力。 如前所述,二氧化硫也存在这种与表面张力的比例关系,因为其相关系数也是正的(表 4)。
当比较具有相似酒精度等级的白葡萄酒和红葡萄酒,即分别含有 12.2% 和 12.3% (v/v) 乙醇的样品 W2 和 R7 时,上述参数的协同作用清楚地显示出来。 由于红葡萄酒样品 R7 中酚类物质的含量增加且蛋白质含量更高,人们预计该样品的表面张力会比白葡萄酒样品 W2 低得多。 然而,红葡萄酒中较高(几乎两倍)的二氧化硫和苹果酸浓度(分别为 106 毫克/升和 1.0 克/升,而分别为 64 毫克/升和 0.6 克/升)使其表面张力值为与白葡萄酒相同(两种情况下均为 46.3 mN/m)。
3.3. 预测模型
如统计分析所示,乙醇、单宁和蛋白质是与表面张力最相关的三个参数。 一方面考虑到它们在酿酒学上的重要性,另一方面考虑到它们的测定方法费力,我们使用回归分析研究了各种数学模型,目的是通过简单的表面测量获得评估其浓度水平的预测模型。紧张。 正如预期的那样,最适合的模型用于估计乙醇含量。 描述它的散点图和线性方程如图 2 所示。该模型将乙醇浓度的变化解释为 91.4%,估计的标准误差等于 0.3 mN/m。
关于蛋白质和单宁,线性预测模型分别仅解释了 48% 和 50% 的方差,与表 4 中给出的 R2 值一致。这个结果意味着对这些参数的预测相当差,尽管蛋白质是表面的-活性分子,而单宁在本研究中与表面张力有很强的相关性; 因此,预计会有更好的结果。 仅为乙醇提供了令人满意的模型的事实可能是由于其在葡萄酒中的含量高,但也可能是因为乙醇值涵盖了图中很宽的浓度范围(11.2-14.2% vol.)(图 2)。 2)。 蛋白质和单宁的情况并非如此,因为在特定样品中,它们的含量值仅涵盖图的两个极端:对于蛋白质,白葡萄酒为 0.081 至 0.140 g/L,红葡萄酒为 0.563 至 0.883 g/L葡萄酒; 白葡萄酒单宁为 0.1 至 0.3 g/L,红葡萄酒单宁为 2.9 至 4.5 g/L(表 2)。 然而,令人鼓舞的是,尽管它们仅基于 20 个样本,但这些预测模型的 R2 分别为 0.4809 和 0.5015。
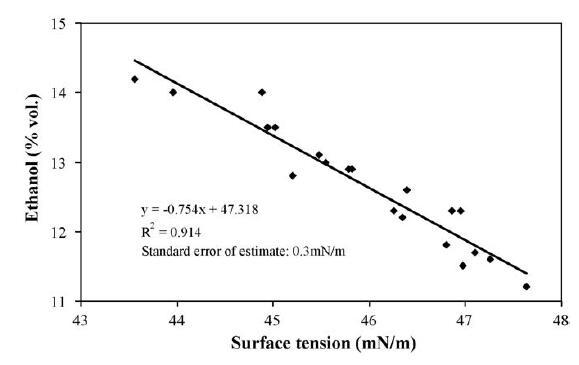
图 2. 根据静止葡萄酒的表面张力预测乙醇浓度的最佳拟合模型图。
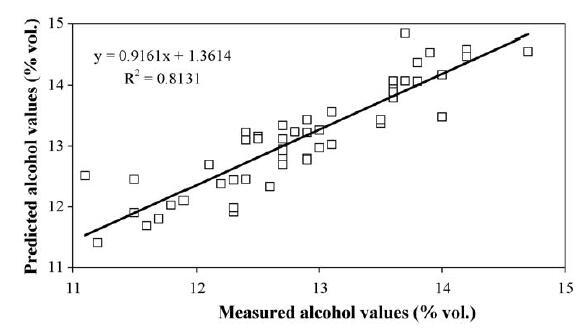
图 3. 50 种静止葡萄酒的酒精强度(% vol.)的预测值与测量值。
为了测试乙醇预测模型,我们分析了第二组 30 个葡萄酒样品。 所提出的线性模型预测的值与葡萄酒酒精度等级的测量值的图如图 3 所示。更新的模型解释了 81.3% 的乙醇含量变化,而现在估计的标准误差为 0.36 % (v/v)。 尽管必须进一步优化,但该统计工具为文献中现有的那些提供了一种额外的方法,用于简单快速地估计静止葡萄酒的酒精等级(Rocchia 等,2007a,b)。
葡萄酒的表面张力与酒本身的成分之间的相关性论文——摘要、简介
葡萄酒的表面张力与酒本身的成分之间的相关性论文——材料和方法










