合作客户/
拜耳公司 |
同济大学 |
联合大学 |
美国保洁 |
美国强生 |
瑞士罗氏 |
相关新闻Info
推荐新闻Info
-
> 五种表面活性剂对粉煤灰基多孔地聚物孔结构与力学性能的调控机制(二)
> 五种表面活性剂对粉煤灰基多孔地聚物孔结构与力学性能的调控机制(一)
> 粉煤灰基多孔地聚物:五种表面活性剂降低碱液表面张力与稳定泡沫的效能对比
> 表面活性剂对粉煤灰基多孔地聚物孔结构及性能的调控机制研究
> 人工模拟瘤胃体外发酵技术:纤维发酵中比表面积与表面张力的调控作用(二)
> 人工模拟瘤胃体外发酵技术:纤维发酵中比表面积与表面张力的调控作用(一)
> 翅果油饮品加工工艺的创新与深度解析界面张力仪在其中的应用
> 基于界面张力最小化优化PS微球制备工艺:SDS与Na₂SO₄浓度的选择
> 表面张力降低视角下离子液体促进气体水合物生成的机理探究
> 低用量、高效率:离子液体促进剂实现水合物生成体系表面张力最大降低53.06%
脂质纳米粒与脂质体的结构差异及其形成机制
来源:百家号 药物递送 浏览 3704 次 发布时间:2022-09-13
脂质纳米粒(Lipid Nanoparticle,LNP)是一种将核酸物质递送至细胞的纳米载体,由可离子化阳离子脂质、中性辅助磷脂、胆固醇、PEG脂质组成。制备过程采用乙醇注入法,将脂质乙醇溶液与核酸物质的酸性(pH=4)水性缓冲液迅速混合,在酸性条件带正电的可电离脂质与带负电的核酸物质静电络合形成纳米粒;再以pH=7.4(高于阳离子脂质的pKa)的水性缓冲液对纳米粒进行透析洗滤,形成完整的脂质纳米粒-核酸递送系统。
文丨塔卡拉玛干的白杨
一、mRNA-LNP的结
关于mRNA-LNP的结构示意图,在认识上存在一定的差异,不同的期刊有不同的结构示意图,甚至同一期刊还有不同的结构示意图。
首先在是Nature系列期刊中,就存在两种明显不同的示意图,有的mRNA-LNP示意图是单层膜结构,而有的文章则描述为双层膜结构。Vaccines和Science期刊中描述的mRNA-LNP示意图则类似于脂质体结构,为双分子层结构。Biotechnology Advances和Journal of Controlled Release期刊则选用了单层膜的mRNA-LNP示意图。
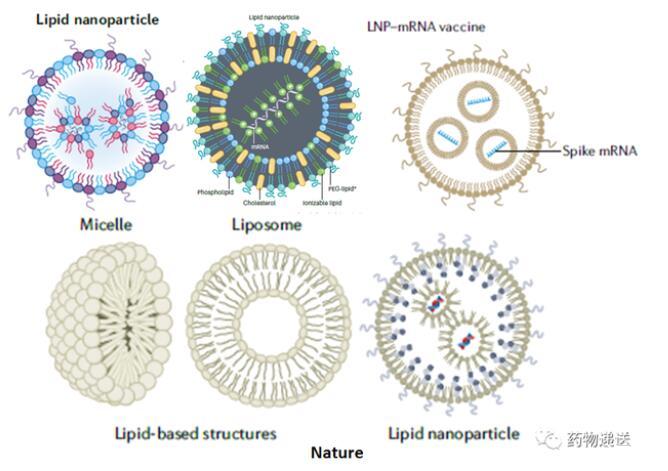
图1 Nature系列期刊的mRNA-LNP结构示意图
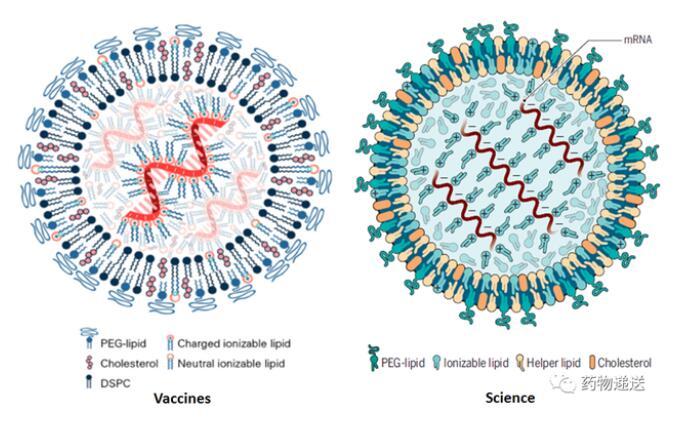
图2 Vaccines和Science期刊的mRNA-LNP结构示意图
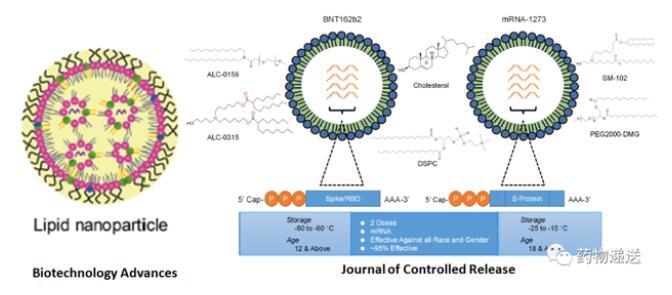
图3 Biotechnology Advances和Journal of Controlled Release期刊的mRNA-LNP结构示意图
Moderna公司描述的mRNA-LNP结构示意图,以及International Journal of Pharmaceutics和Advanced Drug Delivery Reviews期刊描述的mRNA-LNP结构示意图则更为抽象,尤其是International Journal of Pharmaceutics期刊,描述了三种不同的结构。
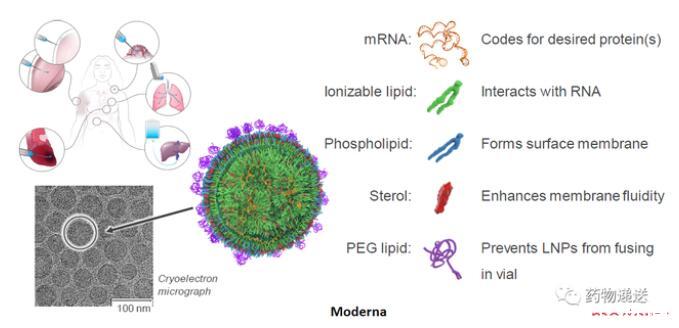
图4 Moderna公司的mRNA-LNP结构示意图
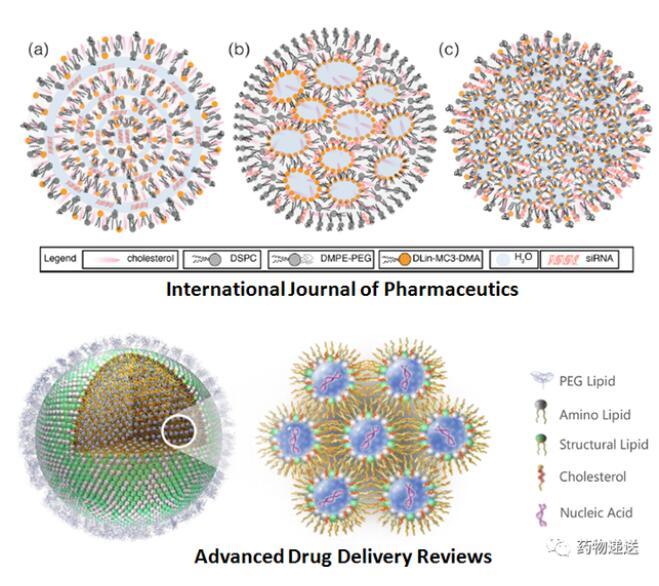
图5 International Journal of Pharmaceutics和Advanced Drug Delivery Reviews期刊的mRNA-LNP结构示意图
笔者认为,mRNA-LNP的脂质膜到底为单层结构还是为双层结构,目前的显像技术尚不能完全区分和识别,但对LNP技术进行溯源,可知其是在脂质体的基础之上发展而来,LNP有包载递送核酸物质的能力而脂质体却不能有效递送核酸物质,主要的区别在于LNP拥有实心内核,能更好地保护核酸物质不提前降解和释放。此外,mRNA-LNP具有的内部核心,其实质是可电离的阳离子脂质与带负电的核酸物质静电作用络合形成复合体,被包载于内部;倘若在不存在核酸物质的情况下,可能形成的就是脂质体,阿米卡星脂质体吸入混悬液便是利用制备LNP微流控技术来生产的。
二、siRNA-LNP的形成机制
关于带电荷脂质和核酸物质包裹形成纳米粒,用于胞内递送的物理过程以及所形成的的结构,目前尚未有统一的认识。
以2018年8月10日FDA批准的Onpartro(Patisiran)为例,其作为首款采用LNP递送siRNA的产品,是诺贝尔奖成果从概念走向临床实际应用的里程碑。LNP-siRNA递送系统是通过快速混合溶解脂质的乙醇溶液和pH=4.0的siRNA水性缓冲液,然后透析去除药液中乙醇并调节pH=7.4,形成LNP-siRNA。通过低温透射电镜观察到,LNP对核酸物质的包载效率接近100%,内部电子密度均匀。分子模型和实验数据表明,LNP是具有包含核酸物质核心的纳米结构。
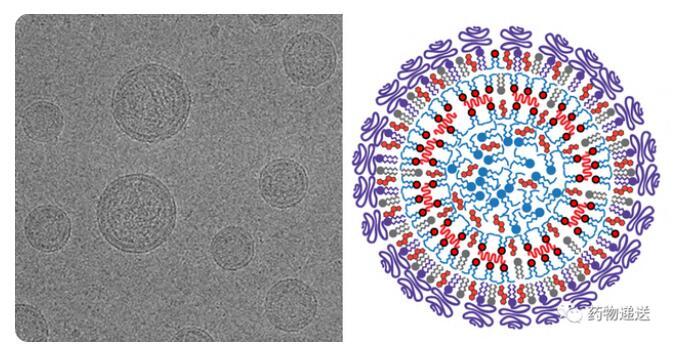
图6 LNP的电镜图和结构示意图
1、形成机制的研究
关于脂质纳米粒的形成,曾经提出过一个“倒置胶束”(inverted micelles)假说,假说认为可电离的阳离子脂质先与核酸物质缔合形成反胶束结构,过量的可电离脂质则形成“空”反胶束;反胶束和“空”反胶束缔合形成疏水核,极性较大的脂质成分(如DSPC)再对疏水核进行包裹。然而,该假说并不能解释脂质纳米粒制备过程中的某些特征现象,例如脂质相和水相快速混合后的LNP-siRNA混悬液在pH=4.0时呈澄清透明,这表明此时脂质纳米粒复合物的结构直径小于30nm;以缓冲液透析置换后LNP-siRNA混悬液呈半透明,表明在此过程中形成了较大结构的脂质纳米粒,也说明脂质纳米粒的粒径在该工艺过程中由小变大。
在此基础上之上,不列颠哥伦比亚大学(Universityof British Columbia)教授彼得卡利斯(Pieter Cullis)对脂质纳米粒的形成过程进行了深入的机制研究。Pieter Cullis教授在40多年前揭开了脂质纳米粒应用的序幕,他的实验室为脂质药物递送系统的发展做出了重要贡献。
相关阅读:详解LNP作为药物递送技术的起源和专利纠纷
Pieter Cullis教授对Onpattro(首款上市的LNP产品)的处方进行了考察,Onpattro的处方为可电离脂质/DSPC/胆固醇/PEG化脂质= 50/10/38.5/1.5(mol/mol),N/P=3。冷冻电镜结果显示,在pH=4的水溶液中,形成的是粒径较小的澄清透明的脂质纳米混悬液;在缓冲液透析和置换的过程中,溶液的pH逐渐升高至7.4,受pH值的驱动,脂质纳米粒在中性水溶液中逐步融合,形成粒径较大的脂质纳米粒,纳米粒的中心形成多层堆叠的固体核心结构。初步估算平均每36个小粒子聚集成一个脂质纳米粒。
此外还发现,采用乙醇稀释/快速混合技术制备LNP-siRNA,当siRNA含量较高时,表现为堆叠的小双层结构,其中siRNA被包载于紧密相连的脂质双分子层之间;当siRNA含量较低时,堆叠结构的比例降低,LNP-siRNA复合物系统则表现出siRNA双层结构和非晶态电子致密核的组合,这可能是由中性形式的可电离阳离子脂质产生的油滴而形成。所得结论为:含可电离阳离子脂质的LNP体系在pH=4时形成双层结构,在pH=7.4时形成非晶态“固体核”结构。
2、影响LNP形成的因素
使用带电荷脂质制备siRNA-LNP时,正电荷与负电荷的数量比会影响纳米粒的大小、稳定性、电位等性能。在siRNA-LNP中,正电荷通常为具有可电离铵根(N)的阳离子脂质,而负电荷则为带有大量磷酸根(P)的核酸分子,两者可通过静电吸附的方式结合在一起。因此,不合理的比例可能会导致粒径过大、稳定性差等缺陷。值得一提的是,在研究中发现,当N/P=1时,pH中和后LNP的粒径不会有较大改变;当N/P=3或者6时,LNP在pH=7.4的缓冲液中粒径会变大。而永久阳离子脂质(例如DOTAP)制备的LNP在任何pH缓冲液中都不具有固体核心结构。
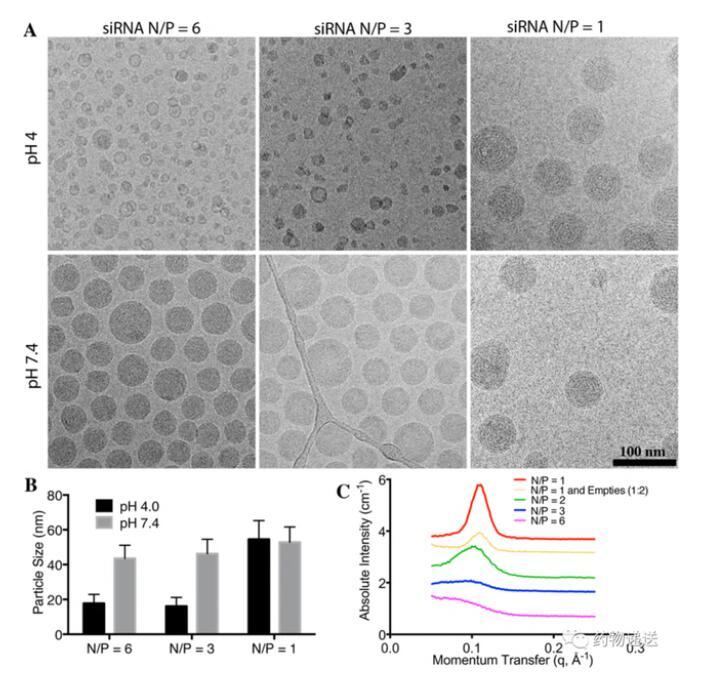
图7 不同的N/P会影响LNP的粒径
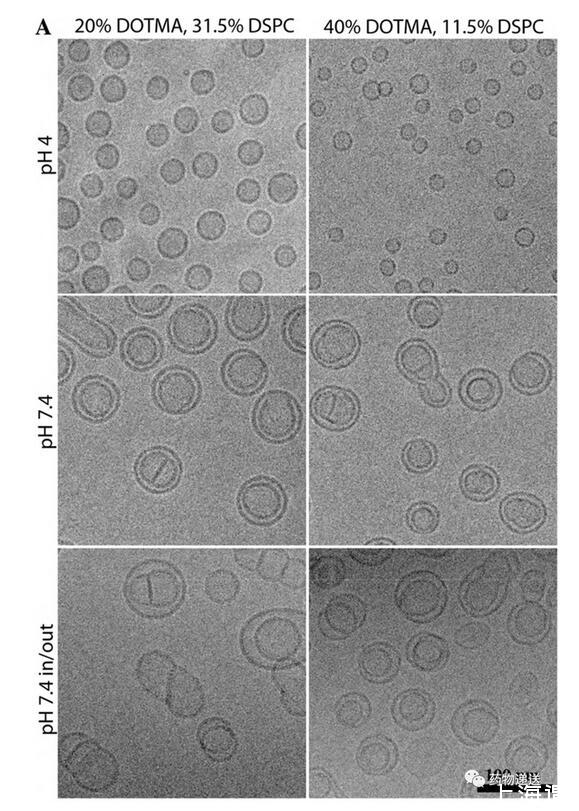
图8 永久阳离子脂质制备的LNP无固态核心
同时研究了siRNA的存在对LNP的形成机制和结构的影响。在没有siRNA存在的情况下,LNP脂质分散体在pH=4.0的条件下快速混合形成粒径较小的单层小泡;随着PBS缓冲液的透析pH值升高至7.4,较多的可电离阳离子脂质以中性形式存在,囊泡间的静电排斥力降低,使得双分子层结构稳定性变差囊泡间产生融合;当小囊泡融合时,PEG脂质、DSPC和胆固醇被分割到越来越大的LNP单外层,而中性的可电离阳离子脂质被分割到LNP的内部并在LNP中心形成油滴相;当外单分子层的PEG脂质浓度足够高时,会抑制LNP之间的继续融合,从而维持平衡态。值得注意的是,虽然平衡态粒径的大小与PEG脂质的浓度有关,但其影响力比DSPC和胆固醇含量的影响要小得多。
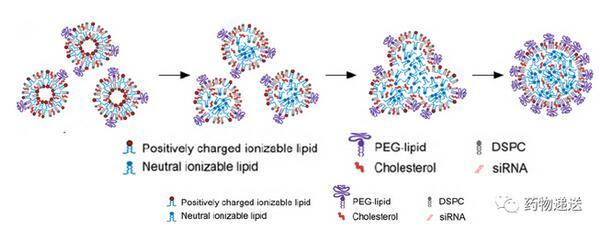
图9 无siRNA情况下LNP的形成
在有siRNA存在的情况下,最初是在紧密相连的脂质单层之间形成包含siRNA的小囊泡;随着pH值的升高,类似于不含siRNA的LNP,可电离脂质电位的中和会诱导脂质颗粒间的融合,这个过程受到复合物中PEG脂质、DSPC和胆固醇的相分离限制;有科学家提出,这些脂质沉积在表面单层,抑制脂质颗粒进一步融合。值得注意的是,高浓度乙醇(体积比不小于25%)会导致除单个脂质分子的高交换率(与siRNA复合的阳离子脂质除外),从而使得快速形成平衡结构;还需要指出的是,必须要有部分DSPC和胆固醇被分割在外单层,并且在pH=4时能维持更小结构的稳定,因为在含有1.5 mol % PEG脂质且没有DSPC或胆固醇的体系中能观察到非常大的微米级系统;随着pH的升高,纳米颗粒经历的过程与不含siRNA时LNP的情况基本相同;可电离脂质向中性形式转化的过程更利于增加在LNP内核中的融合和沉积。
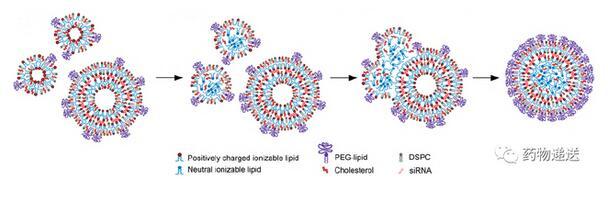
图10 有siRNA情况下LNP的形成
3、结论
LNP-siRNA复合物是通过快速混合-乙醇稀释过程形成,该复合物并没有显示出倒置的胶束结构,其中siRNA以“醋栗小圆面包”(currant bun)的形式分散在LNP内部。相反,siRNA与紧密贴合的脂质双层膜相关,双层脂质膜固定住siRNA分子,分离到LNP的外围。过量的可电离阳离子脂质会形成一个无定形的脂质核心,类似于含有一定量胆固醇的油滴相。
这些研究表明,在优化的LNP-siRNA递送系统中,不同种类脂类的比例可能会根据特定的可电离阳离子脂质而变化。例如,使用KC2脂质时,胆固醇在疏水核中的有限溶解度表明,应降低胆固醇含量以实现更稳定的体系。或者,增加DSPC的用量可能会增强较小的LNP给药系统的稳定性和活性。此前已有研究表明,较小的LNP-siRNA给药系统不如较大的给药系统有效。
三、脂质体和脂质纳米颗粒
脂质体和脂质纳米粒的关键差异,不仅在于他们各自的应用不同,更主要在于他们自身的形态结构、组成和生产工艺存在差异。
从广泛定义来讲,脂质纳米粒是以脂质形成的纳米颗粒,这么划分的话脂质体也是一种脂质纳米粒。然而,在具体的科学研究中,脂质纳米粒是用来描述一种不同于脂质体的特定类型纳米粒。脂质体和脂质纳米粒的最大区别在于形态,脂质体是脂质有序排列的双分子层形成封闭囊泡,有亲水的内部空腔结构;脂质纳米粒则没有亲水空腔,相反,脂质纳米粒因为阳离子磷脂和带负电的核酸物质静电络合作用存在于内部,形成的多层核心分散于脂质层间。
在组成方面,主要成分大致相同,都含有脂质和胆固醇,只是脂质纳米粒所用的脂质中必须要有可电离脂质,而脂质体对脂质的种类没有严格要求。但在各成分的比例方面,脂质体和脂质纳米粒存在较大差异,尤其是胆固醇的用量,以经典的脂质体产品DOXIL为例,HSPC:CHOL:DSPE-PEG2000=3:1:1;而已上市两款mRNA新冠疫苗的组分中,胆固醇分别占比42.7%(Pfizer/BioNTech)和38.5%(Moderna),明显高于脂质体中胆固醇的含量。
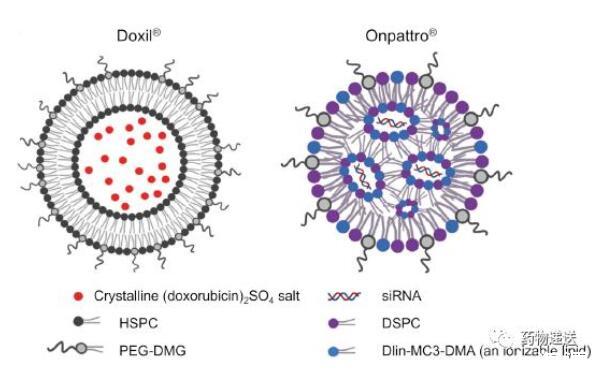
图11 脂质体和脂质纳米粒的差别
在生产工艺方面,脂质体和脂质纳米粒在上游的工艺和步骤是不同的,但下游的生产过程几乎一致。传统的脂质体制备工艺,首先是脂质相和水相形成粗脂质体,再通过均质或挤出工艺将粒径控制在一定的范围内;而脂质纳米粒是利用微流混合系统将脂质乙醇溶液和核酸酸性水溶液快速混合,微流混合系统的连接头可以在两相混合对撞过程中控制粒径。脂质体和脂质纳米粒下游的缓冲液置换工艺几乎一样,都是利用切向流动过滤(Tangential Flow Filtration,TFF)技术进行缓冲液的置换或纯化,最后终端0.22μm滤膜过滤除菌。
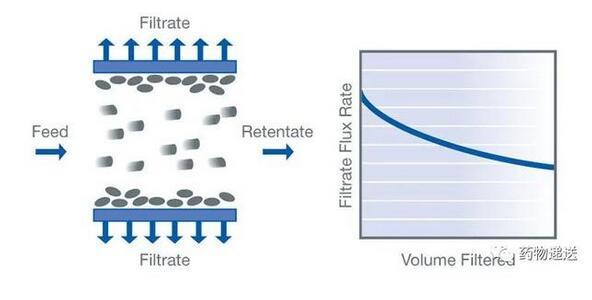
图12 切向流动过滤技术示意图
脂质体和脂质纳米粒同宗同源,脂质体已在药物递送领域扮演重要角色,涉及到众多适应症,而脂质纳米粒目前仅用于核酸物质的递送,希望其在技术的积累和开发下得到广泛应用。










